Há cinco anos, eu passei a trabalhar como membro de um laboratório no Centro Safra para Ética de Harvard, dedicando-me a estudar a “corrupção institucional”. O que eu particularmente apreciei nessa minha passagem pelo laboratório foi que aprendi um método claro para investigar e conceituar o problema. O quadro de referência foi o seguinte: identificar “economias de influência” que podem corromper o comportamento dos indivíduos dentro da instituição, documentar a corrupção e explorar o prejuízo social resultante.
Há cinco anos, eu passei a trabalhar como membro de um laboratório no Centro Safra para Ética de Harvard, dedicando-me a estudar a “corrupção institucional”. O que eu particularmente apreciei nessa minha passagem pelo laboratório foi que aprendi um método claro para investigar e conceituar o problema. O quadro de referência foi o seguinte: identificar “economias de influência” que podem corromper o comportamento dos indivíduos dentro da instituição, documentar a corrupção e explorar o prejuízo social resultante.
Lisa Cosgrove e eu nos juntamos para estudar a “instituição” da psiquiatria através dessa lente, e nos concentramos em seu comportamento institucional desde 1980, quando a American Psychiatric Association (APA) publicou a terceira edição de seu Manual de Diagnóstico e Estatística (DSM). Foi quando a APA adotou o seu modelo de doença para a categorização de transtornos mentais, com a profissão assumindo a tarefa de vender ao público esse novo modelo. Este foi o interesse particular que surgiu em 1980, e que tem moldado seu comportamento desde então. Estamos todos familiarizados com a segunda “economia de influência” que exerceu uma influência corruptora sobre a psiquiatria – dinheiro farmacêutico – mas acredito que a influência da corporação psiquiátrica seja realmente o maior problema.
Em nosso livro Psychiatry Under the Influence, nós documentamos o comportamento corrupto, que poderia ser encontrado em todos os cantos da psiquiatria: a falsa história contada ao público sobre drogas que corrigem desequilíbrios químicos no cérebro; a tendenciosidade dos testes clínicos; a manipulação dos resultados; a ocultação dos resultados pobres de longo prazo; a expansão das categorias de diagnóstico para fins comerciais; e a publicação de diretrizes de pesquisas clínicas que inevitavelmente passaram a promover o uso de drogas psiquiátricas.
No final de nossa investigação, eu tinha uma nova maneira de conceituar o prejuízo social causado por essa corrupção: nossa sociedade se organizou em torno de uma narrativa falsa, que nos foi apresentada como uma narrativa da ciência, mas que é desmentida por um exame atento das provas reais.
Agora, com a publicação de um novo estudo no American Journal of Psychiatry, intitulado “Os efeitos a longo prazo da medicação antipsicótica no curso clínico em esquizofrenia”, temos uma nova oportunidade para observar no artigo esta “mente institucional” da psiquiatria. Escrito pelo ex-presidente da APA Jeffrey Lieberman e outros sete psiquiatras, o artigo pretende servir como uma revisão baseada em evidências para a defesa dos protocolos atuais da profissão para a orientação da prescrição de antipsicóticos, o que inclui o seu uso regular a longo prazo. Examinando atentamente essa revisão, podemos avaliar, uma vez mais, se esta é uma profissão que pode ser confiável para avaliar honestamente sua base de evidências e usar essas evidências para orientar seus cuidados.
O contexto
Em 2010, publiquei Anatomia de uma Epidemia e, nesse livro, escrevi sobre os efeitos a longo prazo dos antipsicóticos, e concluí que há uma história da ciência que leva a essa conclusão: no geral, os antipsicóticos pioram a longo prazo os resultados das pessoas diagnosticadas com esquizofrenia e outros transtornos psicóticos. Joanna Moncrieff escreveu similarmente sobre os perigos dos antipsicóticos em seu livro The Bitterest Pills e em artigos publicados. Assim também Peter Götzsche em seu livro Deadly Psychiatry and Organized Denial e em vários periódicos.
Todas essas críticas ajudaram a promover uma investigação mais aprofundada sobre essa preocupação, o que colocou a psiquiatria em uma situação muito difícil: será que ela prescreve essas drogas de uma forma que causa mais danos do que benefícios? Será que seus protocolos para as drogas – o seu uso imediato para todos os pacientes psicóticos em primeiro episódio e depois o ‘uso contínuo’ das drogas – precisam ser repensados?
Em seu estudo recentemente publicado, Lieberman e colegas realizam o que eles descrevem como uma revisão “baseada em evidências” dessas perguntas. Eles concluem que não há evidência convincente que apoie essa preocupação. Em um subsequente comunicado de imprensa e em um vídeo para Medscape, Lieberman vendeu a ideia de que há provas de que os antipsicóticos fornecem um grande benefício, que os protocolos da psiquiatria são muito bem elaborados, e que os críticos são indivíduos “nefastos” com a intenção de fazer mal.
Joanna Moncrieff já publicou um blog crítico sobre isso no Mad in Brasil, e, em particular, ela chama a atenção para a desistência dos autores em levar em conta os estudos relacionados sobre o efeito dos antipsicóticos nos volumes cerebrais. Miriam Larsen-Barr, que fez pesquisas sobre as atitudes dos usuários em relação aos antipsicóticos, também escreveu um blog criticando o estudo e o comunicado à imprensa, enfocando como os autores ignoram os relatos dos usuários sobre como as drogas afetam suas vidas.
Neste relatório para a comunidade do Mad in America, eu simplesmente quero olhar atentamente como Lieberman e seus colaboradores revisaram a literatura e estudos individuais. Podemos então ver se a fizeram de uma maneira que revela a mente de um grupo interessado em investigar verdadeiramente a questão dos efeitos a longo prazo dos antipsicóticos – com o bem-estar dos pacientes em primeiro plano em seus pensamentos -, ou se revela a ‘mente’ de um grupo interessado em proteger os interesses da corporação.
Então, ao final deste exercício, poderemos fazer esta pergunta essencial:
sendo verdadeiro que não podemos confiar na profissão para o desenvolvimento de tratamentos ‘baseados em evidências’ que coloquem os interesses dos pacientes em primeiro lugar – em oposição aos seus próprios interesses corporativos -, o que a nossa sociedade deve fazer?
Os Autores
Os oito autores se descrevem enquanto “um painel internacional de especialistas em farmacologia antipsicótica, neuroimagem e neuropatologia”. A tarefa que eles próprios se deram foi a de “rever as evidências pré-clínicas e clínicas que apoiam os efeitos adversos potenciais dos antipsicóticos sobre os resultados a longo prazo”.
De uma perspectiva de “corrupção institucional”, há informações adicionais que precisam ser acrescentadas a essa descrição: todos os oito são psiquiatras e, portanto, há um interesse “corporativo” presente nessa revisão, dado que eles estão investigando se um de seus tratamentos é prejudicial a longo prazo. Quanto à influência do dinheiro farmacêutico, cinco dos oito relatam laços financeiros com empresas farmacêuticas, com pelo menos três servindo como palestrantes para múltiplas empresas. Lieberman não relata tais conflitos de interesse, mas ele tem um passado cheio de tais conflitos: em 2009, ele revelou ter tido vínculos financeiros com 15 empresas farmacêuticas nos dois anos anteriores.
As questões
Em sua introdução, os autores citam artigos de Moncrieff, Götzsche e meus que levantam preocupações sobre os efeitos a longo prazo dos antipsicóticos. Em termos de importância clínica, a revisão deve servir como um exame de evidências relevantes para a forma como os antipsicóticos estão sendo prescritos. Estão eles sendo usados de uma maneira que melhor atenda os pacientes, ou de uma maneira que aumenta a probabilidade de que uma pessoa que sofre uma crise psicótica tenha um mau resultado a longo prazo?
O protocolo atual da psiquiatria exige que os medicamentos psiquiátricos sejam prescritos a todos os pacientes psicóticos, bem como a “terapia de manutenção” a longo prazo. Os ensaios controlados com placebo fornecem a evidência para a primeira prática. Estudos de retirada, em que os pacientes estabilizados em medicamentos são randomizados para tratamento continuado ou para retirada (geralmente de forma abrupta), apoiam o segundo (“terapia de manutenção”).
No entanto, os estudos de retirada não mostram como a terapia de manutenção afeta os pacientes a longo prazo. Eles simplesmente revelam que uma vez que uma pessoa tenha sido estabilizada com a medicação, a retirada abrupta da droga é susceptível de levar à recaída. O foco nos resultados de longo prazo, pelo menos como apresentados pelos críticos, fornece evidências de que a psiquiatria deve adotar um protocolo de uso seletivo. Se os pacientes de primeiro episódio não são imediatamente colocados em antipsicóticos, há uma porcentagem significativa que irá se recuperar, e esta “recuperação espontânea” os coloca em um bom processo de longo prazo. Quanto aos pacientes tratados com os medicamentos, o objetivo seria minimizar o uso a longo prazo, pois há evidências de que os antipsicóticos, no seu conjunto, pioram os resultados a longo prazo.
Essa é a relevância clínica dessa “preocupação”. Será que psiquiatria não precisa repensar seus protocolos de uso de drogas para dar aos pacientes a melhor chance para se recuperarem e funcionarem bem a longo prazo?
A boa notícia aqui é que os autores, com esse artigo, estão buscando abordar as principais questões levantadas pelos críticos. Além disso, à medida que realizaram sua revisão, eles revisitaram muitos dos estudos sobre os quais nós “críticos” escrevemos. Em grande medida, eles retraçaram o caminho histórico que eu escrevi em Anatomia de uma Epidemia, que fornece um senso de concordância baseada nas evidências disponíveis e que podem ser revistas.
Desconstruindo sua revisão: Parte um
A primeira parte de sua revisão é dedicada a avaliar a base de evidências para o uso de antipsicóticos para o tratamento de episódios psicóticos, incluindo o seu uso em pacientes de primeiro episódio. Há evidências que deem suporte ao tratamento de todos os pacientes dessa forma? Ou há razão para se desenvolver protocolos, particularmente para pacientes com primeiro episódio, que lhes dariam a oportunidade de se recuperar sem exposição às drogas?
A. Ensaios clínicos controlados com placebo em doentes psicóticos
Em 2009, Leucht publicou uma meta-análise de 38 ensaios clínicos com antipsicóticos de segunda geração, onde ele relata haver uma taxa de resposta de 41% para os pacientes tratados com drogas versus 24% para o grupo placebo. Lieberman e colegas citam esse estudo como fornecendo evidência sólida para a prescrição regular de antipsicóticos a pacientes que experimentam episódios psicóticos. “Esta magnitude do efeito terapêutico é comparável favoravelmente a muitos dos tratamentos eficazes em campos não-psiquiátricos da medicina”, escreveram.
O que está faltando em sua resenha
Embora os estudos controlados com placebo possam mostrar ser um fármaco mais eficaz do que o placebo na redução de um sintoma alvo (durante um curto período de tempo), tais estudos não fornecem evidência do efeito benéfico que o fármaco tem sobre todos os doentes assim tratados. Para fazer essa avaliação, os avaliadores precisam calcular o NNT nos dados do estudo, que é o número de pacientes que precisam ser tratados para obter uma resposta positiva adicional. Isso identifica a porcentagem de pacientes que se beneficiam do tratamento e a porcentagem que pode ser prejudicada pela exposição a um tratamento de que eles não se beneficiam (por exemplo, aqueles que teriam se recuperado de qualquer maneira ou os que não respondem ao tratamento).
Na meta-análise citada por Lieberman, o NNT é 6. Embora 41% dos pacientes tratados com fármaco são respondedores, 24% dos pacientes com placebo também o são, produzindo um aumento líquido nos respondentes de 17%. Isso significa que para cada seis pacientes que você trata com a droga, você receberá uma resposta adicional, e este é o grupo que poderia dizer que se beneficia do tratamento.
Os restantes 83% pertencem à categoria de danos. Há os não-respondedores (59%) que são os que não se beneficiaram com o tratamento, mas que agora estão expostos aos efeitos adversos dos antipsicóticos, e os respondedores ao placebo (24%) que teriam melhorado sem esse tratamento, mas que estão expostos de forma semelhante aos efeitos adversos das drogas.
Se você tiver um tratamento com efeitos colaterais mínimos, então um NNT de seis pode justificar um protocolo de tamanho único. A possibilidade adicional de responder ao tratamento justifica o risco de exposição a um fármaco com efeitos secundários menores. Mas neste caso, uma vez que os antipsicóticos têm tais efeitos colaterais graves, a meta-análise de Leucht de ensaios controlados por placebo fornece um argumento baseado em evidências para evitar antipsicóticos enquanto uma terapia de primeira linha para todos os pacientes, e para se tentar, em vez disso, se outras abordagens – abordagens psicossociais, auxiliares de sono e assim por diante – podem produzir uma taxa de resposta semelhante em curto prazo (41%), sem expor todos aos perigos dos medicamentos. Os fármacos podem então ser tentados como uma terapia de segunda linha para os não-respondedores.
Para os fins deste relatório do Mad in America, a questão é esta: revisores que procuram promover o seu tratamento medicamentoso como efetivo procurarão exclusivamente saber se o tratamento produz uma resposta superior ao placebo. Isso leva a um protocolo totalmente parcial. Por seu turno, os revisores que desejam avaliar o efeito benefício-dano do tratamento em todos os pacientes examinarão os números de NNT. Nesse caso, os cálculos de NNT argumentam para o uso seletivo dos medicamentos, pois o que se busca são protocolos que permitam que “respondedores de placebo” se recuperem sem serem expostos às drogas, e não exijam que os medicamentos sejam prescritos de forma contínua para os “não-respondedores.”
B. Ensaios controlados com placebo em doentes com primeiro episódio
O estudo de Leucht citado por Lieberman implica que 24% dos pacientes psicóticos se recuperarão de um episódio psicótico, ou pelo menos parcialmente, em um período de seis semanas (a duração usual dos ensaios clínicos controlados por placebo). No entanto, os ensaios da meta-análise de Leucht foram realizados em pacientes que haviam sido expostos a antipsicóticos, comparados com o “grupo placebo” composto em sua maioria de pacientes a quem foram abruptamente retiradas as drogas. Eles não são um verdadeiro grupo placebo, e isso levanta uma questão essencial: qual é a taxa de recuperação para pacientes com primeiro episódio que não são tratados com antipsicóticos comparada em relação com a taxa de recuperação para pacientes com primeiro episódio tratados com as drogas?
Em seu artigo, Lieberman e colegas nos dão a resposta: “Nenhum ensaio controlado por placebo com pacientes em primeiro episódio de psicose foi relatado.”
Esta é uma confissão bastante surpreendente. Desde a introdução dos antipsicóticos em 1955, nunca houve um estudo controlado por placebo em pacientes para ver se os fármacos são eficazes neste grupo. No entanto, este tratamento inicial pela via psicofarmacológica regularmente se transforma em um momento decisivo em suas vidas, porque o protocolo usual da psiquiatria é manter os pacientes em antipsicóticos indefinidamente.
Isso por si só deve dar à psiquiatria razão para reexaminar a sua prática para o tratamento de pacientes em primeiro episódio. Essa prática clínica não se baseia em evidências, e parece que a profissão, que gosta de se apresentar como praticante de medicina baseada em evidências, gostaria de remediar essa deficiência extraordinária.
C. Estudos que relataram taxas de recuperação em pacientes com primeiro episódio, ou uma coorte fortemente composta de pacientes em primeiro episódio, que envolveu tratá-los com atenção psicossocial e sem antipsicóticos
1) Odegard e McWalter
Estes são dois primeiros estudos citados por Lieberman e colegas que compararam as taxas de recuperação imediatamente antes e após a introdução de antipsicóticos. Eles escreveram que estes estudos mostraram “aumento das taxas de alta hospitalar e taxas reduzidas de rehospitalização associadas ao tratamento inicial com antipsicótico”.
Com outras palavras, eles estão afirmando que esses estudos apoiam o uso imediato de antipsicóticos em pacientes em primeiro episódio, e que esse uso leva a resultados superiores a longo prazo. Não se trata de evidência controlada por placebo, mas evidência de um tipo diferente que apoia sua prática atual.
O que está faltando em sua resenha
Eles não forneceram quaisquer dados desses dois estudos, que, se apresentados, defenderiam o uso seletivo de antipsicóticos. Aqui estão os dados:
Odegard :

McWalter:
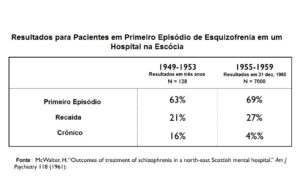
Em ambos os estudos, mais de 60% dos pacientes com primeiro episódio tratados sem antipsicóticos recuperaram e nunca recaíram em períodos de follow-up de três a cinco anos. Eles tiveram um episódio de psicose, ao invés de ficarem cronicamente doentes (e, portanto, de terem que ficar em tratamento contínuo com drogas).
É também notável que a taxa de recuperação – e a taxa de bem-estar de longo prazo – não mudou realmente com a introdução de antipsicóticos. Neste momento, não havia ainda a prática de manter os pacientes fora dos hospitais em tratamento com antipsicóticos, e assim a boa taxa dos que estão bem nesses estudos é para os pacientes que não estão sendo mantidos em medicamentos a longo prazo.
- May
No início da década de 1960, May randomizou 228 pacientes desta forma: os que estavam na primeira admissão para psicoterapia, os que estavam em terapia ambiental (num ambiente de apoio), os que estavam em antipsicóticos, ECT, e os que estavam com drogas mais psicoterapia. Não houve controle de placebo, mas o grupo em terapia ambiental forneceu algo próximo dos que estavam no grupo “os não tratados”. “Pacientes designados para uso de antipsicóticos (sozinhos ou em combinação com outro tratamento) ou ECT passaram menos tempo no hospital nos três anos seguintes e exibiram um funcionamento social superior”, escreveu Lieberman e colegas.
Este estudo está sendo apresentado como a mostrar que o uso inicial do medicamento levou a um melhor resultado no follow-up de três anos para os pacientes assim tratados.
O que está faltando em sua resenha
Eles não conseguiram relatar esse importante resultado: 59% dos pacientes randomizados para a terapia ambiental foram considerados com “sucesso”, e ao longo do folllow-up dos três anos. A respeito May relatou, “os sucessos iniciais do meio funcionaram melhor do que com qualquer outro tratamento, pelo menos no follow-up. ”
De fato, os sucessos com o tratamento em meio psicossocial tiveram as melhores pontuações em qualquer um dos cinco grupos sobre relações sociais e ajuste geral, o que levou May a escrever: “Mesmo que alguns tratamentos psicossociais piorem os resultados em média, seus sucessos podem ser maiores ou sua qualidade mais duradoura.”
Esta é uma descoberta relevante para saber se uma porcentagem significativa de pacientes com primeiro episódio pode ser tratada com sucesso sem medicação e como tais “sucessos” se aplicam a longo prazo. Mais uma vez, mostra que cerca de 60% caíram neste grupo, e que esse grupo de “sucessos” parecia ser de “qualidade mais duradoura”.
- Schooler
No início dos anos 1960, o NIMH realizou um estudo de 229 pacientes com esquizofrenia em fase aguda, que foram randomizados para um de três antipsicóticos ou placebo. Cinquenta por cento eram pacientes em primeiro episódio. Ao passo que, os pacientes tratados com fármaco apresentaram taxas de recuperação mais elevadas a curto prazo, Lieberman e colegas observaram que “os indivíduos que receberam placebo durante o ensaio inicial de 6 semanas tinham menos probabilidade de recaída após a alta hospitalar, em comparação com indivíduos que receberam fenotiazina”.
Depois de ter relatado os melhores resultados de um ano para os pacientes com placebo, em seguida Lieberman e colegas descartaram desta forma esse resultado favorável: “Porque as taxas de abandono são taxas devidas à não-resposta durante o ensaio randomizado inicia, elasl diferiram substancialmente entre os grupos de tratamento (2% com fenotiazina em comparação com 29% no grupo placebo), por isso é altamente provável que a amostra para o estudo de follow-up dos pacientes que receberam alta continha um número desproporcional de pacientes com mau prognóstico no grupo da fenotiazina, uma vez que estes indivíduos não teriam conseguido alta hospitalar se tratados com placebo. ”
O que está faltando em sua resenha
Em primeiro lugar, eles não relataram que 67% do grupo placebo receberam alta e que, portanto, estavam neste grupo de “melhores resultados” no final de um ano. Esta é uma descoberta que parece replicar os resultados no estudo de Mayo.
Em segundo lugar, em seu esforço para descartar os melhores resultados para os pacientes em placebo, Lieberman e colegas assumem que foi o “mau prognóstico” dado aos pacientes placebo que os levou a abandonarem o estudo. No entanto, como mostram estudos longitudinais modernos (como o de Harrow), os desistentes podem ser melhor caracterizados como pacientes “não-conformes”, e este é o grupo que apresenta os melhores resultados a longo prazo.
Em terceiro lugar, quando Schooler procurou explicar os melhores resultados de 1 ano para aqueles tratados com placebo, ele descobriu que os pacientes em placebo eram “mais propensos a ter pais que eram mentalmente doentes”, o que seria um fator de risco que “aumentaria a probabilidade de rehospitalização. ” Esta diferença nos grupos de pacientes, escreveu Schooler,” faria uma maior taxa de rehospitalização de pacientes placebo ser maior, e não menor “.
- Rappaport
Neste estudo de 1970 “com pacientes agudamente psicóticos, a maioria dos quais sem antes haver tomado medicação psiquiátrica”, 127 foram randomizados para placebo ou para clorpromazina, e foram acompanhados (follow-up) por três anos após a alta. Lieberman e colegas escreveram que Rappaport “relatou resultados mais pobres durante um follow-up de 3 anos” no grupo tratado com clorpromazina, mas que depois descartou os melhores resultados para os pacientes placebo.
O projeto, segundo eles, é “confundido por taxas conflitantes desiguais durante a fase inicial de tratamento – 45% dos pacientes tratados com placebo abandonaram-no, comparados com 26% dos pacientes tratados com clorpromazina. Após a correção para a perda desigual de pacientes com mau prognóstico no grupo placebo, as diferenças no resultado não eram mais significativas entre os grupos “.
O que está faltando / errado com a sua revisão
Em primeiro lugar, no final de três anos, havia 41 no grupo placebo que ainda estavam no estudo versus 39 no grupo de drogas. Portanto, não houve “desvio” desigual no final do estudo (ver gráfico abaixo).
Em segundo lugar, Rappaport escreveu que foi “durante o período de follow-up” onde houve um maior peso de indivíduos do grupo placebo, e não na fase inicial do tratamento, como alegou Lieberman.
Se isto for assim, então deveria ter havido um maior peso dos sujeitos do grupo de fármacos na fase de tratamento inicial (para os números em cada grupo serem iguais no final do estudo).
Em terceiro lugar, dos 80 pacientes ainda no estudo ao final, 14 no grupo placebo foram vistos como pacientes com “mau prognóstico” no início do estudo, e 14 no grupo de drogas assim foram designados no início. Assim sendo, não houve “perda desigual de pacientes com mau prognóstico” que tenha levado a confundir os resultados de três anos.
Em quarto lugar, as diferenças nos resultados entre os dois grupos foram impressionantes. Dois terços dos randomizados para placebo estavam fora da medicação no final do período de acompanhamento (follow-up), e foi este grupo que, de longe, teve os melhores resultados em três anos. Ao mesmo tempo, 57% daqueles randomizados para a droga permaneceram com um antipsicótico durante os três anos, e foi este grupo complacente com a medicação – seguindo os protocolos prescritos vigentes para uso de antipsicótico – que teve a mais alta taxa de rehospitalização, cerca de nove vezes maior do que para o grupo nunca exposto.
Aqui estão os resultados que Lieberman e colegas não apresentaram:

Finalmente, em um esforço para investigar a maior taxa de peso para os pacientes placebo na fase de acompanhamento, Rappaport fez esta análise: ele jogou fora os quatro piores resultados no grupo fora de Clorpromazina , e, com este menor tamanho da amostra, passou agora a não haver diferenças significativas entre o grupo nunca medicado e os pacientes randomizados para droga e que depois parou de tomar a medicação durante a fase do follow-up. Rappaport também descartou os cinco piores resultados no grupo com Clorpromazina , mas mesmo com esta manipulação as diferenças significativas nos resultados entre o grupos em placebo / sem Clorpromazina/ e grupos Clorpromazina desapareceram.
Em resumo, Lieberman e colegas, na sua revisão deste estudo, não relataram os seus resultados reais, e descartaram os resultados muito melhores para os grupos fora da medicação, com uma descrição imprecisa da investigação de Rappaport sobre o efeito das taxas de atrito. Lieberman e colegas, no resumo do estudo, declararam que não havia diferenças significativas em três anos entre os randomizados para placebo e aqueles randomizados para droga, quando, de fato, o estudo disse que pacientes em placebo / ou que pararam de tomar saíram-se bem melhor do que aqueles pacientes complacentes com a medicação.
Rappaport deixou isso claro no resumo do estudo: “Nossos achados sugerem que a medicação antipsicótica não é o tratamento de escolha, pelo menos para certos pacientes, se alguém está interessado na melhora clínica de longo prazo. Muitos pacientes não medicados durante o período hospitalar apresentaram maior melhora a longo prazo, menos patologia no follow-up, menos reinternações, e melhor funcionamento geral na comunidade, do que aqueles pacientes que receberam Clorpromazina no hospital “.
- Ran
Lieberman e colegas citaram este estudo chinês em uma seção de seu artigo dedicada a esta pergunta: “Qual é a evidência clínica de que o tratamento inicial afeta resultados a longo prazo?” Nesta seção, eles também citaram Odegard, McWalter, May, Schooler, e os estudos de Rappaport, e assim passam a posicionar o estudo de Ran como um que fornece os achados em pacientes tratados inicialmente com e sem medicamentos, e que são seguidos (follow-up) então por algum tempo.
O estudo de Ran, segundo eles, foi um “follow-up de 14 anos comparando indivíduos medicados com indivíduos nunca medicados”, e descreveram os resultados desta maneira: “Os resultados foram piores no grupo nunca medicado, incluindo as taxas de remissão parcial e completa, falta de moradia e mortalidade. Aproximadamente 10% dos indivíduos que nunca foram tratados obtiveram remissão, e aproximadamente 8% foram parcialmente remitidos, em comparação com 30% e 37%, respectivamente, em indivíduos que regularmente tomaram medicação”.
Dado o contexto, os leitores são induzidos a compreender que esse estudo forneceu a evidência de que o tratamento inicial com medicamento, e o posterior uso “regular” da medicamentação ao longo dos catorze anos, produziram resultados superiores.
O que está faltando / errado com sua revisão
Esse estudo não comparou os resultados a longo prazo de pacientes psicóticos não medicados – com a identificação desses pacientes no início da doença -, com um grupo similar de pacientes medicados. Lieberman e colegas deturparam completamente esse estudo: o seu projeto, a composição das coortes de pacientes, o uso de medicação por eles, e, aparentemente apenas por uma boa medida, os seus resultados.
No estudo, os investigadores de Hong Kong pesquisaram uma comunidade rural da China com 100.000 habitantes, e identificaram 510 pessoas que preenchessem os critérios para um diagnóstico de esquizofrenia. Isso foi em 1994, e em nesse momento do começo da investigação haviam 156 que nunca tinham sido tratados, e 354 que tinham recebido medicação antipsicótica pelo menos uma vez, e que, portanto, foram considerados do grupo “tratado”.
O grupo “não tratado” tinha em média 48 anos de idade e estava doente há 14 anos. Qualquer pessoa desta comunidade rural que, nos anos anteriores a 1994, tivesse sofrido um episódio psicótico e se recuperado sem tratamento, não teria aparecido nesse estudo. Em termos leigos, os pesquisadores identificaram um grupo de pessoas “cronicamente loucas” para comporem o grupo “não tratado” que eles agora seguiriam por 14 anos.
O grupo “tratado” não era, de fato, um grupo “regularmente” medicado, nem mesmo no ponto de partida da pesquisa. Eles eram simplesmente uma coorte de pacientes que haviam recebido medicação antipsicótica pelo menos uma vez antes do início do estudo. Não há informações sobre quantas pessoas neste grupo estavam tomando um medicamento em 1994, quando o estudo começou.
Nesse momento, o grupo crônico, não tratado, estava muito mais doente do que a coorte “tratada”, observaram os pesquisadores. A coorte não tratada era “significativamente de mais velhos, menos propensos a se casar, mais propensos a não ter um cuidador familiar e a viver sozinhos, tinham um nível de escolaridade mais baixo e menos membros da família”. O grupo não tratado também veio de famílias com um nível econômico significativamente com menor status, e com maior probabilidade de haverem sido objeto de violência de suas famílias. Além disso, o grupo nunca tratado teve uma “duração mais longa da doença; maior pontuação média na subescala positiva PANSS; e tinha maior subescala PANSS negativa e de escores mentais em geral. “Oitenta e três por cento tinham sintomas marcantes / ou estavam deteriorados, em comparação com 54% dos do grupo tratado.” Apenas 17% estavam em remissão parcial ou completa na linha de base comparados com os 47% daqueles no grupo tratado.
Nos próximos 14 anos, houve muitos na coorte “não tratada” que continuaram sem tratamento e os pesquisadores relataram a taxa de remissão para esta coorte “nunca medicada” no final do estudo. Quanto ao grupo “tratado”, os pesquisadores não relataram o uso de medicação durante os 14 anos. Eles observam que no último ano do estudo, em 2008, apenas 11% deste grupo “tratado” tomou um antipsicótico de segunda geração, mesmo uma vez. Não há informações sobre se alguém neste grupo estava tomando um antipsicótico de primeira geração naquele momento.
Em sua revisão, Lieberman e colegas não mencionaram isso. Eles apresentam como sendo um estudo de longo prazo que compara indivíduos medicados a não medicados, quando na verdade é um estudo que compara um grupo seleto de pacientes crônicos mais velhos com um grupo menos doente que, em algum momento de suas vidas, foi “tratado”. Pacientes nesta segunda coorte que não estavam tomando um antipsicótico no início e não tomaram qualquer medicação nos próximos 14 anos ainda teriam sido contados nos resultados para o grupo” tratado “. No entanto, Lieberman e colegas descrevem-nos como “regularmente medicados” durante os 14 anos.
Além disso, Lieberman e seus coautores também obtiveram os números de remissão errados. Ao final de 14 anos, a taxa de remissão /remissão parcial para o grupo com doença crônica não medicada foi de 30% (não 18%) e 57% para o grupo tratado (não 67%). Eles deflacionaram a taxa de remissão para o grupo que eles descreveram como “não medicado”, e inflaram a taxa para o grupo que erroneamente foi descrito como “medicado”.
E este é um estudo por eles citado como fornecendo provas de que o tratamento inicial com medicação produziu melhores resultados a longo prazo.
- Seikkula
Nos últimos 15 anos, Jaakko Seikkula tem relatado sistematicamente os resultados de cinco anos com pacientes psicóticos em primeiro episódio e tratados com a terapia do diálogo aberto na Lapónia Ocidental, um protocolo que evita o uso imediato de antipsicóticos. Dois terços de seus pacientes não foram expostos a antipsicóticos ao final de cinco anos e estão assintomáticos e funcionando bem. No entanto, Lieberman e colegas não citam esse estudo, embora ele forneça evidências consistentes com estudos anteriores, de que 60% dos pacientes do primeiro episódio, quando atendidos com assistência psicossocial, podem se recuperar sem o uso de antipsicóticos.
- Estudos de psicose com duração não tratada
Para sustentar seu argumento que o tratamento inicial com antipsicóticos leva a melhores resultados a longo prazo, Lieberman e colegas citaram uma meta-análise de 33 estudos que encontraram “modestas correlações entre uma maior duração da psicose não tratada e sintomas residuais positivos e negativos e prejuízos no funcionamento social.”. Eles também chamaram a atenção para um” estudo quase-experimental “que encontrou uma redução na “diferença entre o início dos sintomas psicóticos e tratamento com antipsicóticos associado com melhores resultados a longo prazo”, com esse estudo durando dois anos.
O que está faltando nessa revisão
Esses estudos sobre a duração de psicose não-tratada não comparam o tratamento inicial de um paciente psicótico em um regime com antipsicóticos com aqueles em um regime sem medicação. Todos os pacientes nesses estudos são tratados com antipsicóticos; a diferença é que um grupo ficou doente por um tempo mais curto do que o segundo grupo antes de entrar em tratamento.
Como Sandy Steingard escreveu em um blog no Mad in America há vários anos, não há uma imagem clara, a partir desses estudos, que se encurtar o tempo da psicose antes do tratamento com um antipsicótico produza uma diferença significativa ao longo de períodos mais longos de tempo. Os resultados têm sido conflitantes. Mas os pesquisadores descobriram sim que um maior atraso para os pacientes receberem cuidados psicossociais leva a uma maior probabilidade de que os pacientes passem a sofrer de sintomas negativos em seis anos.
O tratamento precoce com atenção psicossocial pode produzir um benefício, e talvez o tratamento precoce seja ainda maior se combinado com a ausência de tratamento com neuroléptico.
Desconstruindo sua revisão, parte dois
Na segunda parte do estudo, Lieberman e seus colegas focalizam os “efeitos a longo prazo da medicação antipsicótica no curso clínico da esquizofrenia”. Eles reviram estudos longitudinais, evidências sobre se os antipsicóticos encolhem o cérebro e as preocupações de que os antipsicóticos induzem uma supersensibilidade à dopamina que tornariam os pacientes mais biologicamente vulneráveis à psicose a longo prazo.
A. Estudos longitudinais
- Harrow
Este é o melhor estudo prospectivo, longitudinal, até hoje realizado na era moderna. Com financiamento do NIMH, Harrow acompanhou um grande grupo de pacientes psicóticos, incluindo 64 diagnosticados com esquizofrenia, por mais de 20 anos, e periodicamente foram avaliados os resultados deles, com os pacientes agrupados de acordo com o uso de antipsicóticos. Eis aqui o que Lieberman e colegas escreveram – em sua totalidade – sobre esse estudo, que eles decidiram agrupar, em uma mesma frase, em seu relato sobre um estudo longitudinal finlandês feito por Moilanen.
Os dois estudos, eles escreveram, “encontraram resultados superiores em indivíduos que foram previamente tratados, mas que não tomavam medicação no momento da avaliação, em comparação com indivíduos tomando medicação. No entanto, os pacientes não medicados apresentaram características pré-mórbidas mais favoráveis no estudo de Harrow e colegas, e apresentaram doença menos grave no estudo de Moilanen e colaboradores, sugerindo que em estudos naturalistas não controlados, o status da medicação possa ser em parte o resultado de se os pacientes estão bem ou mal, em vez de ser causa. ”
Em suma, eles reconhecem que os resultados foram “superiores” no estudo de Harrow e também em Moilanen, mas descartaram esses resultados, afirmando que os pacientes não medicados estavam menos gravemente doentes no início.
O que está faltando / errado com a revisão do estudo de Harrow
Não há outro estudo longitudinal na literatura que alcance o nível de Harrow em termos de fornecer dados rigorosos e abrangentes sobre o curso de longo prazo de pacientes psicóticos medicados e não medicados. Ele inscreveu 200 pacientes psicóticos no estudo, provenientes de dois hospitais da área de Chicago (um público e um privado), e eles formavam um grupo de jovens, com uma idade média de 22,9 anos. Quase metade eram pacientes com o primeiro episódio, e outros 21% tinham apenas uma internação prévia. Todos foram convencionalmente tratados no hospital com medicamentos e, após serem dispensados, Harrow realizou um acompanhamento regular que identificasse o uso de medicamentos, seus sintomas e seu funcionamento. Ele dividiu seus pacientes em diferentes subgrupos: pacientes esquizofrênicos com bom prognóstico e com mau prognóstico, e pacientes com distúrbios mais leves. No final de 15 anos, ele ainda tinha 77% dos 200 pacientes no estudo, o que é uma façanha extraordinária. Em estudos sobre drogas, as taxas de abandono em testes clínicos, mesmo de curto prazo, são muito maiores do que as da pesquisa de Harrow.
No entanto, Lieberman e colegas, em um artigo que se propunha investigar os efeitos a longo prazo dos antipsicóticos, não apresentam detalhes que possam dizer sobre o rigor deste estudo, e eles não apresentam nenhum dos dados de desfecho. Além disso, sua explicação para os pacientes não medicados – que era porque supostamente tinham um melhor prognóstico inicial – é desmentida pelos dados de Harrow, e a razão para que isso possa ser mostrado é precisamente porque Harrow dividiu os pacientes em grupos com prognósticos diferentes.
Para os doentes não medicados, verificou-se uma enorme diferença nos resultados, em todos os domínios, que começaram com o follow-up de 4,5 anos e permaneceram durante todas as avaliações subsequentes. Para aqueles com diagnóstico de esquizofrenia, a taxa de recuperação a longo prazo para o grupo sem medicação foi de 40% contra 5% para o grupo medicado. Os pacientes não medicados estavam muito mais propensos a trabalhar, tinham melhores resultados em testes cognitivos e tinham menos ansiedade em cada avaliação de acompanhamento. Talvez o mais notável de tudo, eles eram muito menos propensos a ter sintomas psicóticos em cada follow-up, começando com a avaliação feita em 4,5 anos. Aqui estão os resultados que Lieberman e colegas não apresentaram e nem discutiram:
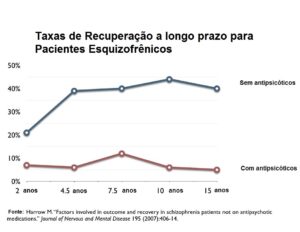




Tendo falhado em apresentar esses dados, Lieberman e colegas, em seguida, descartaram os “resultados superiores” para os pacientes não medicados, afirmando que este grupo tinha mais “características favoráveis premórbidas”. Há uma história interessante por trás desta explicação para a diferença de resultados, que a psiquiatria tem se agarrado – mesmo depois que foi revelado ser falsa.
Harrow, em seu relatório de 2007, levantou a hipótese para os melhores resultados no grupo sem medicação a uma diferença nas características premórbidas, visto que os pacientes com bom prognóstico estariam mais propensos a parar a medicação. No entanto, essa explicação foi desmentida bem em seguida: os pacientes com bom prognóstico de esquizofrenia que deixaram a medicação ficaram melhor do que os pacientes com bom prognóstico de esquizofrenia que permaneceram tomando antipsicóticos, e isso foi verdadeiro para todos os outros subgrupos (pacientes com prognóstico ruim que deixaram de tomar a medicação estavam melhor do que os pacientes com mau prognóstico que permaneceram com a medicação, e que era o mesmo para aqueles com distúrbios psicóticos mais leves). E o mais impactante de tudo: os pacientes esquizofrênicos que pararam de tomar antipsicóticos ficaram melhor do que aqueles com transtornos mais leves que continuaram a tomar os medicamentos.

Em suas publicações mais recentes, Harrow reconheceu que isso é assim mesmo. Em cada subgrupo, os grupos em medicação apresentaram resultados significativamente piores a longo prazo. Em um artigo de 2013, ele resumiu seus pensamentos desta maneira:
“Como é tão patente que a aparente eficácia dos antipsicóticos possa diminuir ao longo do tempo ou se tornar ineficaz ou prejudicial? Há muitos exemplos de outras medicações de efeitos semelhantes a longo prazo, e isso frequentemente ocorrendo porque o corpo se readapta biologicamente aos medicamentos.”
2. Moilanen
Como mencionado acima, Lieberman e colegas citam este estudo no trabalho de Harrow e descarta-o na mesma frase, afirmando que os pacientes não medicados estavam menos gravemente doentes no início do estudo.
O que está faltando / errado com este comentário
Neste estudo, pesquisadores finlandeses identificaram 70 pacientes nascidos em 1966 que foram diagnosticados com psicoses esquizofrênicas. Eles avaliaram o estado dos pacientes em 2000, quando tinham 34 anos de idade (com uma duração média de doença de 10,4 anos). Naquela época, os 24 pacientes fora da medicação estavam muito melhor do que os 46 pacientes com antipsicóticos: eles tiveram uma maior probabilidade de estar trabalhando, maior probabilidade de estar em remissão, e tendo melhores resultados clínicos. Em suma, não foi que o grupo não medicado neste estudo estivesse “menos gravemente” doente quando inicialmente diagnosticado, mas sim que uma década após o diagnóstico inicial, aqueles fora de medicação estavam indo muito melhor do que aqueles em medicação.

Os pesquisadores então seguiram os 70 pacientes por mais nove anos, e aqueles que usaram antipsicóticos menos de 50% do tempo estiveram mais propensos a funcionar bem, estar em remissão e ter um bom resultado clínico.
Como foi o caso com a apresentação do estudo de Harrow, Lieberman e colegas não relataram esses dados, e eles explicaram por que os “resultados superiores” não foram levados em consideração com uma alegação de que o grupo não medicado era menos gravemente doente – o que não é o encontrado no próprio estudo.
3. Wils
Há outro estudo longitudinal que fornece dados de resultados a longo prazo tomando como base pacientes em uso de antipsicóticos. Trata-se de um estudo dinamarquês de 496 pacientes com espectro de esquizofrenia de primeiro episódio e diagnosticados entre 1998 e 2000. Ao final de 10 anos, havia 303 pacientes ainda no estudo, 121 dos quais eram considerados “não-complacentes” e fora da medicação. Não houve diferenças na linha de base entre os grupos não-complacentes e em medicação em 10 anos.
Aqui estão seus resultados de 10 anos:

Este estudo não foi citado por Lieberman e colegas.
- Tiihonen
Em sua revisão de estudos longitudinais, Lieberman e colegas gastaram apenas uma frase para abordar os estudos de Harrow e Moilanen, não citaram o estudo dinamarquês e, em seguida, escreveram que “outros estudos naturalistas encontraram melhores resultados em indivíduos com esquizofrenia em comparação com aqueles que não tiveram esses bons resultados”. Eles não deram detalhes desses outros estudos naturalistas, mas citaram dois relatos de Tiihonen e seus colegas finlandeses.
O que há de errado com este comentário
Os artigos de Tiihonen não são estudos de resultados, e não são estudos de específicos pacientes conhecidos. Ambos são relatórios de um grupo finlandês que vasculhou um registro nacional de prescrições de drogas para relatar as taxas de recaída e mortalidade de pacientes psicóticos, organizadas pelo seu atual uso de antipsicótico.
No primeiro estudo, identificaram 2230 adultos hospitalizados em um primeiro episódio de esquizofrenia de 1995 a 2001 e, em seguida, registraram o uso de medicação por cada período de 30 dias após a alta (com base em uma base de dados nacional para prescrições de antipsicóticos). Qualquer recaída ou morte durante um período de 30 dias foram marcadas como sendo resultados para o antipsicótico particular que estava sendo tomado, ou marcado como “não antipsicóticos” se eles não receberam uma prescrição durante esse mês. Dada esta metodologia, qualquer um que saiu de um medicamento e teve recaída apareceria nos resultados para “nenhum antipsicótico”, e se alguém cometeu suicídio após a interrupção de um medicamento, isso também foi registrado como os resultados de “sem antipsicóticos”. Eles descobriram que havia um maior risco de recidiva durante meses de “sem medicação”, que, tanto quanto qualquer coisa, pode ser devida ao alto risco que vem quando se é colocado em um antipsicótico e, posteriormente, se tenta sair dele.
No segundo estudo deste mesmo grupo, eles relataram taxas de mortalidade de pacientes com esquizofrenia com base no tempo de exposição a antipsicóticos ao longo de um período de 11 anos. Os pesquisadores relataram que “o tratamento de longo prazo com drogas antipsicóticas está associado com menor mortalidade em comparação com nenhum uso de antipsicóticos”. Eles fizeram isso examinando o mesmo banco de dados de prescrições de antipsicóticos nas diversas regiões do país.
Embora não seja um estudo de resultados, este estudo tem sido citado como evidência de que o uso prolongado de antipsicóticos reduz a mortalidade na esquizofrenia. No entanto, como os críticos deste estudo descobriram, as mortes de pacientes hospitalizados não foram contadas, o que levou a uma exclusão de “64% das mortes com antipsicóticos em uso.” Além disso, o grupo com a menor taxa de mortalidade, de longe, foi com aqueles que usaram antipsicóticos pelo período de menos de seis meses ao longo dos 11 anos, em oposição àqueles que usaram antipsicóticos regularmente.
Como tal, os estudos de Tiihonen não podem ser descritos como “estudos naturalistas” que encontraram “melhores resultados” em pacientes medicados. Não foram estudos de pacientes conhecidos; eles não traçaram os resultados durante períodos mais longos de tempo (gravidade dos sintomas, cognição e medidas funcionais); e há razões para se argumentar que as taxas de mortalidade foram mais baixas entre aqueles pacientes que usaram antipsicóticos apenas por um curto período de tempo.
B. Encolhimento cerebral
Lieberman e colegas revisaram uma série de estudos sobre os efeitos dos antipsicóticos sobre os volumes do cérebro, e se essas alterações estão associadas com o agravamento clínico, o declínio cognitivo e danos funcionais. A conclusão a que chegaram pode ser resumida desta maneira:
- Não está claro se o encolhimento cerebral visto em pacientes com esquizofrenia ao longo do tempo é devido à droga ou à doença.
- Não está claro se essa perda de substância cinzenta em pacientes com esquizofrenia está associada com piora clínica, comprometimento cognitivo ou comprometimento funcional.
- O assunto precisa de um estudo mais aprofundado.
O que está faltando em sua resenha
Um esforço para avaliar os efeitos a longo prazo dos antipsicóticos requer, acima de tudo, ver se as evidências de diferentes tipos se encaixam. A questão dos seus efeitos a longo prazo surge dos estudos longitudinais: por que os pacientes “não medicados” em Harrow, Molainen e Wils têm melhores resultados a longo prazo e em cada domínio medido? A crença convencional tem sido que os antipsicóticos são um tratamento essencial, ainda que os dados longitudinais desmintam essa crença. Isso leva a uma busca de pesquisa que possa fornecer uma explicação biológica para os resultados observados nos dados longitudinais.
Os dados de encolhimento cerebral precisam ser vistos sob essa luz. O que a pesquisa mostra? Há evidências de vários pesquisadores, nos EUA e no exterior, de que os antipsicóticos encolhem o cérebro, e que esse encolhimento está relacionado à dose. O mesmo efeito neurotóxico pode ser observado em estudos em ratos e macacos, e nesses estudos em animais o encolhimento não pode ser atribuído à doença. E, como Joanna Moncrieff observou em seu blog em resposta ao artigo de Lieberman, “não há estudos que mostrem alterações progressivas do cérebro em pessoas diagnosticadas com esquizofrenia ou psicose na ausência de tratamento antipsicótico”.
Existem também estudos que descobriram que este encolhimento se correlaciona com aumento dos sintomas positivos, aumento dos sintomas negativos e diminuição da cognição e do funcionamento. Estudos longitudinais relatam piores resultados para pacientes medicados, e os estudos com ressonância magnética relatam drogas que reduzem o volume cerebral, e que esse encolhimento está associado a piores resultados. Os dois conjuntos de dados combinam-se para contar uma história coerente.
Em seu blog, Moncrieff fornece uma crítica detalhada da revisão por Lieberman e colegas da literatura de encolhimento cerebral. Mas o maior fracasso deles na apresentação dessa pesquisa pode-se dizer haver começado na parte inicial do seu artigo, quando não conseguiram apresentar os resultados dos três estudos longitudinais e fingiram que os dois artigos publicados por Tiihonen representavam estudos naturalistas que encontraram melhores resultados a longo prazo para pacientes medicados. Eles nunca apresentaram os dados longitudinais que combinam com a pesquisa de encolhimento cerebral, e que apresentam evidências convincentes de que o uso a longo prazo desses medicamentos piora os resultados agregados.
Ainda assim, apesar de não terem apresentado os dados longitudinais, a revisão que eles fizeram da pesquisa cerebral ainda os levou a um pântano intelectual. Como poderia ser que a redução nos volumes cerebrais observada em pacientes psicóticos estava relacionada inteiramente com a doença e não com os fármacos, quando o encolhimento também se manifestou em animais tratados com as drogas? Eles chegaram a esta explicação: “A relevância” de tais achados “é incerta, devido a diferenças relacionadas às espécies e porque os animais não têm a fisiopatologia da esquizofrenia”.
Com essa explicação, eles estavam criando a noção de que as drogas que encolhem o cérebro normal não afetam o cérebro “psicótico” da mesma maneira, e isso os levou a especular se a redução nos volumes cerebrais observada em pacientes com esquizofrenia, mesmo se devida à droga, é uma coisa ruim. Sim, em pessoas normais a perda de matéria cinzenta correlaciona-se com uma queda no QI, mas talvez tenha o efeito oposto em pessoas com diagnósticos psicóticos. “É possível que os antipsicóticos possam ter efeitos deletérios sobre o cérebro normal, mas efeitos protetores na presença de neuropatologia relacionada à esquizofrenia”.
C. Hipersensibilidade à dopamina
No final da década de 1970, Lieberman e colegas escrevem, surgiu a preocupação nos círculos de pesquisa psiquiátrica de que os antipsicóticos induziam uma hipersensibilidade à dopamina – uma mudança na densidade dos receptores da dopamina – que poderia tornar os pacientes mais vulneráveis às recaídas do que no curso normal de sua doença. Isso poderia explicar por que as taxas de recaída sejam tão altas nos estudos de abstinência e por que tantos pacientes tratados com antipsicóticos se tornam cronicamente doentes.
Lieberman e colegas reconhecem que os antipsicóticos induzem um “rápido aumento na densidade do receptor D2”. Mas, segundo eles, dois estudos de retirada fornecem razões para duvidar de que este é um problema. Em um deles, a velocidade de diminuição das doses (abrupto versus gradual) não produziu diferentes taxas de recaída para os pacientes retirados, e, em um segundo relatório, uma meta-análise de estudos que haviam mapeado recaída após a retirada, os investigadores descobriram que os pacientes retirados continuaram a ter recaída em uma taxa bastante estável ao longo do primeiro ano, ao mesmo tempo que, entre os pacientes medicados, a diferença nas taxas de recaída, entre os dois grupos, foi sustentada ao longo dos doze meses.
Com tal literatura de retirada havendo sido tomada por eles como guia, Lieberman e colegas concluíram que “os estudos clínicos não forneceram provas convincentes de que o tratamento com antipsicóticos piora o curso da doença, que aumenta o risco de recaída ou que causa déficits cognitivos”.
O que está faltando em sua resenha
Como foi o caso com a questão do encolhimento cerebral, qualquer investigação da hipersensibilidade à dopamina induzida por drogas precisa começar com dados de resultados que tiveram essa preocupação logo no começo. Na década de 1970, os relatos de taxas mais elevadas de recidiva de longo prazo para pacientes medicados, em comparação com pacientes não tratados com antipsicóticos, que foram encontrados nos estudos por Schooler, Bockoven, Rappaport, Mosher e Carpenter, apresentaram o campo com um enigma. Os estudos de retirada que eles realizaram mostraram que os pacientes retirados dos fármacos recaíram a uma taxa muito mais elevada do que os doentes mantidos com fármaco. Isso permitiu concluir que os medicamentos reduziam o risco de recidiva. Mas os dados do resultado contaram maiores taxas de recaída para os pacientes medicados! Como explicar este enigma?
Isso levou Carpenter a formular uma profunda pergunta: E se os pacientes nunca tivessem sido colocados em drogas desde o começo? Talvez as drogas induziram uma mudança biológica que tornou os pacientes mais biologicamente vulneráveis à psicose. Isto poderia conduzir a um risco aumentado da recaída após a retirada da droga, que apareceria nos estudos da retirada. No entanto, se os pacientes permanecessem nos medicamentos, a hipersensibilidade à dopamina que é induzida por drogas poderia levar a um risco aumentado de que eles se tornassem cronicamente doentes. Isso explicaria os maus resultados para os pacientes medicados nos estudos longitudinais. Os estudos de retirada podem não haver mensurado o retorno de uma doença, mas sim mostrado o risco da saída de uma droga após o cérebro do paciente haver sido alterado por ela.
Chouinard e Jones deram uma explicação biológica para o que parecia estar acontecendo. Os fármacos bloqueavam os receptores da dopamina e, em resposta ao bloqueio, havia o aumento da densidade dos receptores da dopamina, tornando os pacientes mais biologicamente vulneráveis à psicose. Eles realizaram estudos em seus pacientes que confirmaram sua teoria, e concluíram que essa mudança induzida por drogas poderia levar a mais “sintomas graves” do que em pacientes que nunca tinham experimentado antes essas drogas.
Essa foi a pesquisa que publicada no início dos anos 80, e os modernos estudos longitudinais, que encontraram taxas de remissão mais altas em pacientes não medicados a longo prazo, fornecem novas evidências para apoiar a conclusão de que a hipersensibilidade à dopamina induzida por drogas aumenta o risco de uma pessoa ficar cronicamente doente (ver Harrow, Moilanen e Wils). Para investigar especificamente esta questão, Harrow relatou sobre sintomas psicóticos durante um período de 20 anos para aqueles que permaneceram tomando antipsicóticos ao longo do estudo, comparando-os com aqueles que nunca tomaram qualquer medicação a partir do segundo ano. Aqui estão os resultados:

Essa é a história da hipersensibilidade à dopamina. Mas Lieberman e colegas não apresentaram esse contexto histórico, e eles não mencionaram os dados longitudinais modernos, ou a investigação de Harrow sobre isso. Eles não apresentaram as pesquisas que demonstram de forma convincente que a hipersensibilidade à dopamina induzida por drogas pode piorar os resultados a longo prazo.
Tudo está bem na terra da psiquiatria
 O que pode ser visto aqui, nesta desconstrução da revisão por Lieberman e colegas, é que eles apresentaram informações, uma vez mais, de uma forma que protege os interesses corporativos da psiquiatria e seus protocolos atuais para a prescrição de antipsicóticos.
O que pode ser visto aqui, nesta desconstrução da revisão por Lieberman e colegas, é que eles apresentaram informações, uma vez mais, de uma forma que protege os interesses corporativos da psiquiatria e seus protocolos atuais para a prescrição de antipsicóticos.
- Eles nunca fornecem dados dos estudos mostrando que cerca de 60% dos pacientes em primeiro episódio podem se recuperar sem o uso de antipsicóticos.
- Eles sempre descartam os melhores resultados para pacientes não medicados em estudos citados, argumentando que é um artefato de uma comparação desigual por alguma razão ou outra (Schooler, Rappaport, Harrow e Moilanen).
- Eles não relatam dados de estudos longitudinais modernos que mostram resultados muito melhores a longo prazo para os pacientes não medicados.
- Em suas discussões sobre o encolhimento do cérebro induzido pela droga e a hipersensibilidade à dopamina, eles falham em discutir informações de um corpo maior da literatura científica essencial para avaliar se esses efeitos podem explicar os pobres resultados a longo prazo observados nos estudos longitudinais.
Depois de revisar a literatura dessa maneira protetora da corporação, Lieberman e colegas tiraram essas conclusões:
- Há “pouca evidência” de que o uso inicial de antipsicóticos ou o tratamento de manutenção com as drogas tenham um “efeito negativo a longo prazo”.
- Há apenas um “pequeno número” de pacientes que podem “se recuperar de um primeiro episódio de psicose sem tratamento farmacológico ou que possa interromper a medicação e permanecer estável por longos períodos de tempo”.
- Estudos clínicos randomizados (Leucht) e estudos de retirada de fármacos “apoiam fortemente a eficácia dos antipsicóticos no tratamento agudo da psicose e na prevenção da recaída”.
Eles compõem um “grupo internacional de especialistas”, e chegaram a uma conclusão reconfortante para a corporação psiquiátrica: Os protocolos de uso de drogas que a profissão vem usando há décadas estão bem.
O Comunicado à Imprensa (e denúncia pública dos críticos)
Em nosso livro Psychiatry Under the Influence, Lisa Cosgrove e eu escrevemos sobre o dever de uma profissão médica para avaliar honestamente e relatar as evidências de seus tratamentos em revistas médicas e para comunicar essas informações de forma precisa ao público. O artigo publicado por Lieberman e colegas no American Journal of Psychiatry serviu como a sua comunicação para a profissão médica; enquanto que um comunicado feito à imprensa em 5 de maio, pela Columbia University Medical, serviu como a sua comunicação para o grande público.
O comunicado à imprensa merece ser desconstruído também, pois ele aumenta o relato de uma narrativa que apoia os interesses corporativos. Os autores são descritos como um grupo internacional de especialistas, que conduziram esta revisão para responder a críticos que estavam levantando preocupações sobre antipsicóticos que tinham o potencial de “enganar alguns pacientes (e suas famílias)”, e, portanto, levá-los a “recusar ou descontinuar o seu tratamento com antipsicótico “. Após a realização de um” exame completo “de todas as provas possíveis, eles fizeram uma conclusão definitiva:” Para pacientes com esquizofrenia e distúrbios psicóticos relacionados, medicamentos antipsicóticos não têm efeitos negativos a longo prazo sobre os resultados dos pacientes ou o cérebro. Além disso, os benefícios destes medicamentos são muito maiores do que seus potenciais efeitos colaterais. ”
Se alguém ousar duvidar dessa descoberta, Lieberman disse no comunicado de imprensa que “deve conversar com pessoas cujos sintomas foram aliviados pelo tratamento e que tiveram literalmente as suas vidas devolvidas”.
As drogas foram mais uma vez lançadas como essenciais e até mesmo como agentes milagrosos (“salva-vidas”), e isso se tornou a narrativa promovida por eles junto ao público, e repetida em histórias publicadas pela Agência Internacional de Notícias (UPI) e em sites como Science Daily e Medical News Today. Enquanto isso, Lieberman também elogiou a importância do artigo em um vídeo no Medscape, descrevendo-o como um “grande desenvolvimento em psiquiatria”. Vestido com um casaco branco, ele disse que o estudo “chegou a uma conclusão muito firme sobre o benefício inquestionavelmente positivo dessas drogas “, e então ele apontou aqueles que ousaram questionar seus méritos em primeiro lugar.
Tais foram as comunicações de Lieberman e do Centro Médico da Universidade de Columbia, e há poucos dias eu recebi um e-mail de um amigo na Islândia, que tem sido um ativista na comunidade de usuários há algum tempo, que perfeitamente resumiu seus efeitos sobre as crenças sociais.
“Eu estava falando com alguns doutores noutro dia,” escreveu. “Eles estavam muito entusiasmados com um artigo recém-publicado. Muitos médicos de muitos países contribuíram para esta pesquisa e a linha de fundo era que os remédios são bons e eles certamente estão ajudando “.
O dano feito
Em seu vídeo, Lieberman fala sobre críticos “semeando sementes de inverdades” e como tais “inverdades” podem causar danos; e eu tenho que concordar que semear sementes de inverdades pode causar danos. Podemos vê-lo tão claramente neste caso de corrupção institucional.
Os estudos que relatam que 60% dos pacientes não medicados em primeiro episódio estão em recuperação e que os melhores resultados a longo prazo são de longe aqueles entre pacientes que não estão medicados, são trabalhos que falam de uma oportunidade para a psiquiatria compreender: que os psiquiatras poderiam mudar seus protocolos e dar uma chance para as pessoas que sofrem de um episódio psicótico para se recuperar e prosseguir bem com suas vidas sem os muitos efeitos adversos dos antipsicóticos. Existe uma “base de evidência” que fala de novas possibilidades para as pessoas assim diagnosticadas.
Mas Lieberman e colegas não apresentaram essa possibilidade nesta revisão. Pelo contrário, eles as esconderam da vista. Essa é uma ação que faz mal a milhões de “pacientes” e suas famílias, e assim a toda a sociedade. Continuaremos a viver numa sociedade organizando seus cuidados – e suas leis em relação aos pacientes psicóticos – em torno de uma narrativa falsa, contada para servir os interesses corporativos da psiquiatria, em vez dos melhores interesses dos pacientes.
O desafio para a nossa sociedade
Em um estudo sobre corrupção institucional, o objetivo final é apresentar ideias para resolver a corrupção. Lisa Cosgrove e eu, reconhecemos, tivemos muitas dificuldades com esta seção do nosso livro.
Embora os problemas em psiquiatria venham se tornando bem conhecidos por nossa sociedade, o foco da sociedade tem sido em restringir a influência farmacêutica sobre a psiquiatria. Mas como pode a influência de seus interesses corporativos ser freada?
Eu realmente não sei. O problema é que o poder reside na corporação psiquiátrica e em seus psiquiatras acadêmicos, que escrevem artigos como este. Eles têm a reputação na sociedade de serem especialistas; seus artigos são publicados em “revistas médicas”; e eles têm acesso à imprensa. O site da comunidade Mad in America (em parceria com Mad in Brasil e Mad in America para hispanohablantes) é destinado a servir de fórum para criticar essa narrativa convencional, e estou esperançoso de que os psiquiatras na Islândia não estarão falando em breve sobre as “inverdades” semeadas pelo artigo de Lieberman no American Journal of Psychiatry.
Mas eu tenho um desejo. Gostaria que todos os residentes psiquiátricos se familiarizassem com essa controvérsia, e lessem os artigos de pesquisa que foram citados, e então perguntem a si mesmos: este relatório publicado, o comunicado de imprensa que se segue e o vídeo de Lieberman são o trabalho de uma profissão médica a qual nós podemos nos orgulhar de estar fazendo parte?
Ou eles são o trabalho de uma profissão médica que precisa ser completamente refeita, e este refazer ir ao encontro das necessidades de saúde mental das pessoas em todos os cantos do mundo? Isso poderia ser um legado para uma nova geração de psiquiatras.





 Há cinco anos, eu passei a trabalhar como membro de um laboratório no Centro Safra para Ética de Harvard, dedicando-me a estudar a “corrupção institucional”. O que eu particularmente apreciei nessa minha passagem pelo laboratório foi que aprendi um método claro para investigar e conceituar o problema. O quadro de referência foi o seguinte: identificar “economias de influência” que podem corromper o comportamento dos indivíduos dentro da instituição, documentar a corrupção e explorar o prejuízo social resultante.
Há cinco anos, eu passei a trabalhar como membro de um laboratório no Centro Safra para Ética de Harvard, dedicando-me a estudar a “corrupção institucional”. O que eu particularmente apreciei nessa minha passagem pelo laboratório foi que aprendi um método claro para investigar e conceituar o problema. O quadro de referência foi o seguinte: identificar “economias de influência” que podem corromper o comportamento dos indivíduos dentro da instituição, documentar a corrupção e explorar o prejuízo social resultante.











 O que pode ser visto aqui, nesta desconstrução da revisão por Lieberman e colegas, é que eles apresentaram informações, uma vez mais, de uma forma que protege os interesses corporativos da psiquiatria e seus protocolos atuais para a prescrição de antipsicóticos.
O que pode ser visto aqui, nesta desconstrução da revisão por Lieberman e colegas, é que eles apresentaram informações, uma vez mais, de uma forma que protege os interesses corporativos da psiquiatria e seus protocolos atuais para a prescrição de antipsicóticos.
 A revista Schizophrenia Bulletin publicou recentemente um estudo sugerindo que níveis mais elevados de comportamento sedentário e inatividade física estão associados a pior desempenho cognitivo em pessoas diagnosticadas com esquizofrenia. Aqueles com baixos níveis de comportamento sedentário curiosamente apresentaram melhor tempo de reação motora e processamento cognitivo em níveis significativos.
A revista Schizophrenia Bulletin publicou recentemente um estudo sugerindo que níveis mais elevados de comportamento sedentário e inatividade física estão associados a pior desempenho cognitivo em pessoas diagnosticadas com esquizofrenia. Aqueles com baixos níveis de comportamento sedentário curiosamente apresentaram melhor tempo de reação motora e processamento cognitivo em níveis significativos.

 Em 17 de fevereiro de 2017, Lancet Psychiatry publicou um
Em 17 de fevereiro de 2017, Lancet Psychiatry publicou um