Depois que Joanna Moncrieff e colegas publicaram seu estudo desmascarando a teoria da depressão baseada na baixa serotonina, o editor de Mad na Suécia, Lasse Mattila, escreveu ao Conselho Nacional de Saúde e Bem-Estar Social da Suécia, perguntando se este estudo afetaria as diretrizes nacionais da Suécia para o tratamento da depressão. Eis como o Conselho Nacional respondeu:
“O estado do conhecimento sobre os efeitos antidepressivos dos ISRSs não se baseia em teorias de [seus] mecanismos de ação, mas em estudos clínicos comparando os efeitos de medicamentos em pacientes com placebo. Portanto, o artigo não altera o estado do conhecimento sobre os efeitos antidepressivos clínicos dos ISRSs ou a base para a recomendação de antidepressivos nas diretrizes nacionais para transtornos de depressão e ansiedade”.
A diretoria nacional sueca está apontando para uma conclusão simples: ensaios aleatórios, controlados por placebo e pelo duplo-cego descobriram que os antidepressivos são “eficazes”, e é por isso que a diretoria recomenda o seu uso para tratar a depressão e a ansiedade. Em nível nacional, os medicamentos são vistos como um benefício positivo para a saúde pública.
Este é o mesmo entendimento “de base” que tem impulsionado a prescrição de antidepressivos nos Estados Unidos e em grande parte do mundo desenvolvido. Os ensaios aleatórios controlados por placebo (RCTs) são vistos como o “padrão ouro” para avaliar a eficácia de um tratamento medicamentoso, e seus resultados são percebidos na sociedade como fornecendo uma conclusão binária: ou um medicamento é comprovadamente eficaz ou não é. Se for o primeiro, então se entende que a presença desse medicamento entre os recursos disponíveis de um país sirva a um propósito de saúde pública: o medicamento deve ajudar a amenizar a carga de depressão e ansiedade na saúde pública.
Esta confiança nos RCTs como a palavra final sobre a eficácia dos antidepressivos – como se o Deus da ciência tenha estendido seu longo dedo e os declarado bons – é facilmente demonstrada como tendo produzido um público iludido sobre seus méritos e alheio aos danos que eles têm causado a nível de saúde pública.
Para entender por que isto é assim, basta investigar esta questão: Na natureza, muitas vezes existe uma capacidade natural de recuperação de uma “doença”. Será que os antidepressivos melhoram essa capacidade natural de recuperação?
Como até mesmo uma rápida revisão revela, os RCTs de antidepressivos não fornecem provas disso. Mesmo os dados limitados que eles fornecem são de qualidade duvidosa, uma vez que vêm principalmente de ensaios financiados pela indústria, e as descobertas não são preditivas dos resultados em cenários do “mundo real”.
A consagração dos RCTs, na verdade, leva a um tipo de cegueira social e médica. A comunidade psiquiátrica – e, por extensão, nossa sociedade – se concentra em um único aspecto dos dados arrancado dos RCTs: a diferença na “redução dos sintomas” entre grupos de medicamentos e placebo no final do período de estudo (normalmente seis semanas.) As metanálises de experimentos descobriram que a diferença média é “estatisticamente significativa”, e isso se torna fundamental. Esta conclusão permanece mesmo quando os pesquisadores apontam que a diferença nos sintomas é tão pequena que não tem significado clínico; que vem de ensaios que são tendenciosos de múltiplas maneiras; e que quando a exposição a eventos adversos é adicionada à equação risco-benefício, a maioriao dos pacientes sofre danos com o tratamento.
Essa é a miopia que ocorre quando os resultados dos RCTs são resumidos. Talvez ainda mais problemáticos são os achados de outros tipos de estudos – uma história de pesquisa que se estende por mais de 50 anos e que fala de antidepressivos piorando os resultados a longo prazo – que são descartados porque não provêm de um RCT. E voilá! Com os antolhos firmemente instalados, nosso fetiche pelo RCT leva a pronunciamentos definitivos de que os antidepressivos “funcionam”.
Esta mentalidade se tornou visível em 2018, quando um grupo internacional de pesquisadores publicou uma meta-análise de 522 ensaios aleatórios de 21 antidepressivos na revista Lancet. A análise deles foi centrada nas diferenças na redução dos sintomas no final dos ensaios de curto prazo e, embora os pesquisadores tenham concluído que havia um “risco moderado a alto de viés” em 82% dos ensaios, e que a diferença na redução dos sintomas fosse bastante pequena, eles concluíram que todos os 21 “eram mais eficazes do que placebo”.
Jornais e outros meios de comunicação tiraram a sua conclusão : Este estudo havia provado, de uma vez por todas, que os antidepressivos funcionam.
Esta foi a conclusão a que o Conselho Nacional de Saúde e Bem-estar da Suécia se referiu quando declarou que os estudos clínicos apoiavam sua recomendação de antidepressivos como um tratamento para a depressão. Os RCTs tinham mostrado isso, e essa era toda a evidência que precisava ser considerada.
RCTs em psiquiatria
A adoção do estudo “randomizado, bem controlado, duplo-cego” como padrão-ouro para avaliar os medicamentos data do final dos anos 40, quando os investigadores britânicos usaram um projeto de randomização para avaliar a eficácia da estreptomicina como tratamento para a tuberculose pulmonar. A randomização forneceu uma imagem clara dos benefícios do medicamento, e na década seguinte as variáveis “bem controladas” e o “duplo-cegos” foram adicionados à randomização para criar esta “metodologia de padrão-ouro”.
A reificação pela sociedade dos RCTs veio em 1962, quando a FDA começou a exigir que as empresas farmacêuticas provassem à FDA que seus medicamentos não eram apenas seguros, mas eficazes também. As provas de eficácia, declarou a FDA, deviam vir de “estudos adequados e bem controlados”.
Como método para avaliar a eficácia de um tratamento para uma doença infecciosa, um RCT tem valor óbvio, e muitas vezes pode emitir um juízo definitivo. Entretanto, mesmo antes que a FDA acrescentasse a exigência de eficácia, entendia-se que a aplicação desta ferramenta aos medicamentos psiquiátricos teria seus desafios. O RCT nasceu como uma forma de avaliar a eficácia de um tratamento para uma doença específica, mas os pacientes diagnosticados com esquizofrenia ou depressão não eram conhecidos por compartilharem uma patologia comum. Havia preocupações de que os medicamentos psiquiátricos, devido a seu efeito sobre os estados emocionais internos, levariam a uma quebra dos “fatores de controle” e do “duplo-cego” dos ensaios, e isto levaria a resultados tendenciosos. Mais importante, não estava claro como os resultados poderiam ser medidos, dado que não havia marcadores biológicos de “doença” que pudessem ser avaliados.
Entretanto, uma vez que a FDA adotou seu padrão de eficácia, tais preocupações foram postas de lado.
A psiquiatria teria que adotar um modelo de doença para testar seus medicamentos. Os psiquiatras desenvolveram “escalas de classificação” para fornecer uma medição numérica dos sintomas que se dizia serem característicos da depressão e outros transtornos psiquiátricos e, uma vez isso ocorrido, os antolhos sociais foram fixados firmemente. As escalas de classificação, naturalmente, não teriam a precisão que as medições de doenças físicas podem ter, e também seriam subjetivas por natureza, e, não obstante, o uso de uma escala viria a gerar um número específico e, de repente, uma pontuação de 14 em uma escala de classificação de 52 pontos poderia ser vista como uma avaliação precisa dos sintomas de um paciente deprimido.
Os ingredientes para uma miopia institucional estavam agora estabelecidos. A FDA, a profissão psiquiátrica e a sociedade considerariam a redução dos sintomas a curto prazo como evidência da eficácia de um medicamento, e mesmo que um medicamento psiquiátrico o fizesse apenas em um grau ligeiramente melhor do que “placebo”, ele seria considerado eficaz. O ensaio clínico de seis semanas seria uma prova de que o uso do medicamento na sociedade proporcionava um benefício.
RCTs controlados pela indústria
Antes dos anos 80, as empresas farmacêuticas tinham que vir literalmente com “chapéu na mão” para pedir aos médicos acadêmicos que conduzissem os seus ensaios. As bolsas do NIH eram a moeda do reino da medicina acadêmica antes daquela época, e os médicos acadêmicos, se concordassem em realizar os ensaios de medicamentos, insistiriam em projetar os ensaios, analisar os resultados e publicar os resultados. A independência dos médicos acadêmicos proporcionava uma segurança científica para os ensaios.
Por diversas razões, essa independência começou a desaparecer durante os anos 80, e isso foi particularmente verdadeiro na psiquiatria. O primeiro ISRS a chegar ao mercado foi o Prozac em 1988, e naquela época as empresas farmacêuticas já haviam afirmado o controle dos RCTs de seus medicamentos psiquiátricos, e isso se mantém desde então. As empresas farmacêuticas projetam os ensaios, analisam os resultados e decidem quais os resultados publicar.
Os resultados que emergem dos RCTs de antidepressivos servem às empresas farmacêuticas de duas maneiras: eles fornecem dados para aprovação pelo FDA e os resultados “estatisticamente significativos” que podem ser usados para comercializar os medicamentos. A questão importante para a sociedade é esta: Qual a relevância desses resultados para a prática clínica e sua contribuição para uma “base de evidências” para o uso desses medicamentos?
Nenhuma comparação com “resultados na natureza”
O grupo placebo em um ensaio com drogas deve representar os resultados que ocorrem no “curso natural da doença”. Entretanto, nos RCTs de antidepressivos, os pacientes que atualmente tomam tais medicamentos são regularmente inscritos e depois passam por uma brusca suspenção da medicação antes da randomização para o medicamento e o placebo.
Como tal, o grupo “placebo” é melhor descrito como um grupo de retirada de drogas. Assim, os ensaios não fornecem informações sobre a capacidade natural dos pacientes deprimidos de melhorar a curto prazo, e como os RCTs podem alterar essa taxa natural de recuperação. Para que os RCTs forneçam essa informação, os pacientes inscritos nos ensaios precisam ser virgens de medicação ou pelo menos estar sem antidepressivos por um longo período.
Os voluntários do estudo não são representativos de pacientes do “mundo real”
Para que os RCTs sejam úteis, eles devem fornecer evidências dos efeitos do medicamento em pacientes que serão receitados em ambientes clínicos. Entretanto, em ensaios de medicamentos psiquiátricos, as empresas farmacêuticas utilizam critérios de inclusão e exclusão para selecionar os pacientes mais propensos a responder bem ao tratamento. Os critérios de exclusão em ensaios com antidepressivos podem incluir comorbidades psiquiátricas, abuso de álcool, pensamentos suicidas e uma não resposta a um antidepressivo anterior.
Um relatório de 2005 da Câmara dos Comuns no Reino Unido resumiu esta deficiência nos RCTs:
“Os ensaios em humanos tendem a ter um valor preditivo limitado devido a problemas de extrapolação para a prática clínica de rotina. Tipicamente, apenas uma pequena amostra da população em perspectiva a ser exposta ao medicamento pode ser estudada em ensaios clínicos. Além disso, os pacientes que provavelmente serão expostos ao medicamento se ele for comercializado podem ser excluídos dos ensaios clínicos porque têm múltiplas patologias ou tomam uma série de medicamentos diferentes”.
Estudos descobriram que 60% a 90% dos pacientes do “mundo real” estão excluídos dos ensaios de antidepressivos financiados pela indústria. Isto levou John Rush, psiquiatra do Texas Southwestern Medical Center em Dallas, a observar em um artigo de 2004 que “os resultados clínicos a curto e longo prazo de pacientes externos representativos com transtorno depressivo maior não psicótico tratados na prática diária, tanto no setor privado quanto no público, ainda não estão bem definidos”.
O uso de medicações concomitantes confunde os resultados
Um RCT é projetado para isolar o efeito do medicamento específico que está sendo testado. Entretanto, em testes antidepressivos, o uso de medicamentos concomitantes é comum.
Esta prática apareceu no primeiro ISRS aprovado para comercialização (Prozac.) Nos ensaios clínicos iniciais da fluoxetina, os investigadores notaram que o medicamento estava induzindo “acatisia e inquietação” em uma porcentagem significativa de pacientes. Em resposta, Eli Lilly emendou seus protocolos para permitir “o uso de benzodiazepinas para controlar a agitação”. Os ensaios estavam agora testando esta possível combinação de drogas psiquiátricas, e como Dorothy Dobbs, de Eli Lilly, confessou mais tarde em tribunal, o uso de benzodiazepinas era “cientificamente ruim”, pois “confundiria os resultados” e “interferiria na análise tanto da segurança quanto da eficácia.”[1]
Entretanto, uma vez que a FDA aprovou o Prozac, as empresas farmacêuticas entenderam que esta prática “cientificamente ruim” seria agora aceitável. Em um artigo de 1997, os pesquisadores escreveram que “o uso concomitante de medicamentos é uma prática comum na maioria dos ensaios clínicos com medicamentos antidepressivos”.
A prática continua até hoje. Nos ensaios de vortioxetina, aprovados para comercialização em 2013, o protocolo permitia “o uso ocasional de zolpidem, zopiclone e zaleplon para insônia”. Três das 17 perguntas da Escala de Classificação Hamilton para Depressão (HRSD) avaliam a insônia, com pontuação coletiva para as três perguntas variando de 0 a 6. O uso concomitante de um comprimido para dormir no ensaio poderia reduzir este número, e assim ajudar a aumentar a “eficácia” do antidepressivo.
Isto significa que a eficácia do RCT não pode ser atribuída apenas ao antidepressivo, mas sim à combinação de medicamentos.
Os viéses do Projeto
As empresas farmacêuticas querem que os ensaios clínicos produzam resultados que ajudem seus novos medicamentos a ter sucesso no mercado. Seu objetivo não é um objetivo científico, mas sim de marketing.
Há inúmeras maneiras pelas quais as empresas farmacêuticas buscam atingir este objetivo. Elas podem projetar ensaios que favoreçam o medicamento e minimizem a evidência de efeitos colaterais, publicar apenas os ensaios que produzem resultados positivos, e fazer girar esses resultados.
Como observado acima, nos ensaios com antidepressivos, os pacientes que tomaram antidepressivos e outros medicamentos são inscritos no estudo e estes medicamentos são, então, retirados de forma bastante abrupta. Os ensaios freqüentemente empregam uma fase de “introdução ao placebo” antes da randomização. Aqueles que melhoram durante esta fase – por exemplo, os que respondem com placebo – não são randomizados no estudo. Esta exclusão dos que respondem a placebo produz uma coorte inteira de pacientes que podem estar apresentando sintomas de abstinência na “linha de base”, e a randomização os separa em um grupo de placebo que pode continuar a apresentar tais sintomas, e em um grupo colocado de volta em um medicamento similar ao que eles tinham tomado.
Em um trabalho de 2019, os investigadores do Nordic Cochrane Centre concluíram que este projeto poderia ter três efeitos sobre os resultados do estudo:
- Os participantes tratados com a droga em estudo, ou uma droga similar, antes da inclusão e posteriormente randomizada para a droga, muito provavelmente a tolerarão e experimentarão menos danos em comparação com uma população sem drogas (danos reduzidos no grupo da droga).
- Os sintomas de retirada no grupo placebo podem ser mal interpretados como sinais de agravamento da depressão ou como eventos adversos (redução dos benefícios e aumento dos danos no grupo placebo).
- Os participantes já tratados com um antidepressivo e posteriormente randomizados para o medicamento em estudo podem ter experimentado sintomas de abstinência durante a entrada em placebo que são então aliviados pelo medicamento em estudo. Pode ser mal interpretado como uma melhora da depressão, em oposição a um alívio dos sintomas de abstinência (aumento dos benefícios no grupo do medicamento).
Um protocolo pode incorporar qualquer número de elementos projetados para produzir resultados favoráveis ao medicamento. Por exemplo, um protocolo pode procurar reduzir a evidência de efeitos colaterais exigindo que os pacientes relatem espontaneamente os efeitos colaterais, ao invés de fazer com que os investigadores perguntem aos pacientes sobre tais sintomas. Ou mesmo se for utilizada uma lista de verificação de sintomas, a lista pode não incluir eventos adversos que surgiram durante os estágios iniciais dos testes, mas que não fazem parte dos efeitos colaterais conhecidos desta classe de drogas.
A FDA está bem ciente deste viés. Os revisores da FDA de “Novas Formas de Uso de Drogas” frequentemente apontam as formas em que os testes são tendenciosos em favor do medicamento do fabricante, ou como os possíveis efeitos colaterais foram minimizados. A tomada de consciência desta agência apareceu nas revisões da FDA sobre o Prozac.
Em seus resumos escritos sobre a fluoxetina, os revisores da FDA observaram que sua eficácia sobre o placebo era marginal, e que era menos eficaz que o medicamento comparador nos ensaios, a imipramina. Sua revisão dos relatos de casos revelou que a fluoxetina poderia causar uma longa lista de efeitos colaterais preocupantes -psicose, mania, insônia, nervosismo, confusão, tontura, disfunção de memória, tremores e coordenação motora prejudicada – e eles puderam ver que mesmo esta lista de efeitos colaterais era incompleta. Eli Lilly, escreveu David Graham, da FDA, tinha “participado em grande escala da subnotificação” dos danos que a fluoxetina poderia causar. [2] Outro revisor, Richard Kapit, apresentou esta conclusão de fundo: a fluoxetina “pode afetar negativamente os pacientes com depressão “[3].
Entretanto, a FDA deu ao Prozac seu selo de aprovação e, ao fazê-lo, estabeleceu um padrão para a aprovação de antidepressivos pela agência: mesmo que os medicamentos tivessem sido mal administrados em testes, ou mesmo que a empresa tivesse procurado esconder os efeitos adversos, a FDA lhe daria luz verde.
De fato, quando a Pfizer procurou a aprovação da sertralina (Zoloft), os revisores da FDA observaram que ela não havia demonstrado eficácia em quatro dos seis ensaios, que havia um quinto que era “questionável”, e que apenas um que era positivo. Paul Leber, da FDA, ao mesmo tempo em que insistia que o Comitê Consultivo de Drogas Psicofarmacológicas da FDA aprovasse a sertralina, confessou que não tinha “nenhuma idéia do que constitui prova de eficácia, exceto o que nós, como Comitê, concordamos, de forma ad hoc [base], que precisa haver”. O Comitê Consultivo, acrescentou ele, “poderia nos dizer: ‘olha, nós achamos que os padrões neste campo são terríveis'”. [4]
Tudo isso é bem conhecido. Em uma meta-análise de 2017 de 131 RCTs de antidepressivos, pesquisadores dinamarqueses concluíram que todos os 131 “estavam com alto risco de viés”. Os investigadores do Nordic Cochrane Collaboration Center, que analisaram novamente os dados dos 522 estudos do estudo Lancet, concluíram que não havia nenhum que estivesse livre de um risco de viés, e que havia um “alto risco de viés” em 414 ensaios. Como resultado, concluíram que a “certeza da evidência” na metanálise Lancet era “muito baixa”.
Os antidepressivos não proporcionam um benefício clinicamente significativo acima do placebo
O resultado primário em RCTs de antidepressivos concentra-se em uma única medição: Ao final do estudo (geralmente seis semanas), os sintomas no grupo dos antidepressivos diminuíram mais do que no grupo dos placebo, e verificar se a diferença é estatisticamente significativa.
Relatórios de ensaios financiados pela indústria apresentam regularmente um gráfico que parece mostrar uma diferença notável na redução dos sintomas entre o antidepressivo e o placebo. Aqui, por exemplo, um gráfico que mostra os resultados de um ensaio americano de vortioxetina, que foi aprovado pela FDA em 2013. Os sintomas foram medidos na Escala de Depressão Montgomery-Asberg de 60 pontos (MADRS).

Este gráfico, após exame minucioso, mostra que os sintomas diminuíram cerca de 14,4 pontos para aqueles a quem foram dados 20 mg de vortioxetina, 13,0 pontos no grupo de 10 mg, e 10,8 no grupo de placebo. A diferença de 3,6 pontos entre a dose de placebo e 20 mg foi estatisticamente significativa e, portanto, evidência da eficácia do medicamento a essa dose. (A dose de 10 mg não passou o corte “estatisticamente significativo”).
Entretanto, o gráfico serve como uma ilusão de eficácia. A diferença de sintomas é traçada contra um eixo de 18 pontos e, em lugar da escala MADRS completa de 60 pontos. Os pesquisadores determinaram que uma diferença de 6 pontos nos escores MADRS é a “diferença mínima” que é clinicamente significativa (ou mesmo clinicamente perceptível.) Se você traçar os resultados com uma escala de 60 pontos, você pode ver imediatamente porque isto é assim.
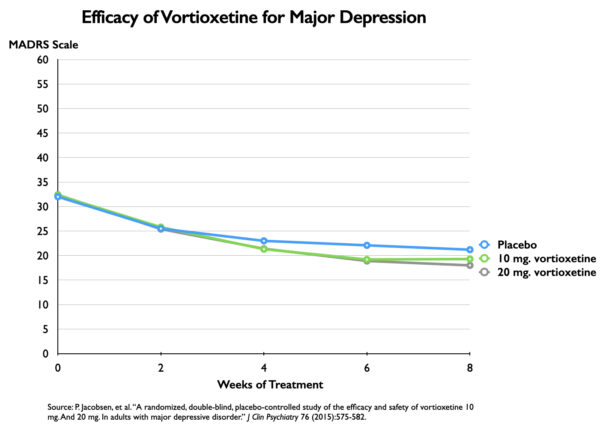
Esta falta de significado clínico tem se mostrado repetidamente em meta-análises de ensaios com antidepressivos. Em 2008, Irving Kirsch e colegas revisaram 47 ensaios de quatro ISRSs, e constataram que havia uma redução média de 9,6 pontos no HRSD de 52 pontos no grupo de antidepressivos, e 7,8 pontos no grupo de placebo, uma diferença de 1,8 pontos. O Instituto Nacional de Excelência Clínica estabeleceu uma diferença de 3 pontos no HRSD como a diferença mínima que poderia ser vista como clinicamente significativa.
As meta-análises mais recentes chegaram à mesma conclusão. O estudo dinamarquês de 131 ensaios encontrou uma diferença média de 1,94 pontos, que, observaram os investigadores, “estava abaixo de nosso limiar predefinido de significância clínica de três pontos”. O Centro Nórdico Cochrane, em sua revisão do documento da Lancet, determinou que a diferença média entre o medicamento e o placebo seria de 1,97 pontos. Eles também observaram que “os clínicos são incapazes de detectar reduções na escala de classificação de depressão Hamilton de três pontos ou menos”.
Assim, a própria meta-análise que os jornais alardearam como provando, de uma vez por todas, que os antidepressivos funcionam, na verdade, falava de uma diferença, entre o medicamento e o placebo, tão pequena que os clínicos não seriam capazes de notá-la, e isto estava em testes conhecidos por serem tendenciosos contra o placebo.
A maioria dos pacientes em RCTs continua deprimida
Embora os pacientes tratados com um antidepressivo no RCT apresentem uma redução nos sintomas, no final, a maioria permanece deprimida. Por exemplo, no ensaio de vortioxetina, a pontuação média do MADRS para aqueles que receberam a dose de 20 mg – a dose que foi considerada eficaz – foi de 18. Esta pontuação está no topo da faixa de pontuação para depressão leve (pontuação 7 a 19).

Embora Kirsch e colegas em seu relatório de 2008 não tenham fornecido uma pontuação composta de pontuação final para os pacientes em sua meta-análise, eles relataram pontuação final em 35 dos ensaios, e se a média dessas pontuações, a média para o braço antidepressivo é de 16,0, ela é categorizada como “leve a moderadamente deprimida”.
As análises de tamanho de efeito revelam que 8 de 9 pacientes tratados com um antidepressivo sofrem “danos”
Os dados do RCT, quando cuidadosamente analisados, fornecem um método para avaliar uma equação de “benefício/ dano” para os pacientes. Kirsch, os investigadores dinamarqueses e outros calcularam que a diferença de 2 pontos nos sintomas equivale a um tamanho de efeito de 0,3. Um tamanho de efeito de 0,3 significa que há uma sobreposição de 88% no espectro de resultados para o grupo do medicamento e placebo.

Um cálculo relacionado que os investigadores fazem é o “número necessário para tratar” (NNT): quantos pacientes devem ser tratados com um medicamento para produzir uma resposta adicional além do placebo? Com um tamanho de efeito de 0,3, que se traduz em um NNT de 9. Assim, a equação de risco/benefício que emerge dos RCTs de antidepressivos: Um dos nove pacientes receberá um benefício além do placebo. Os outros oito não receberão nenhum benefício adicional, mas estão expostos aos efeitos adversos do medicamento. Isto os coloca na categoria “prejudicados”. A natureza dos possíveis danos pode ser vista em uma compilação dos efeitos adversos do medicamento, juntamente com os perigos associados ao uso de antidepressivos a longo prazo.
O ponto de partida
Como pode ser visto, os RCTs de antidepressivos não fornecem provas de que os antidepressivos “funcionam”.
Não há comparação com resultados em pacientes não tratados; ensaios financiados pela indústria produzem relatos exagerados de eficácia; os resultados não são vistos como preditivos de resultados em cenários do mundo real; o grupo placebo é um grupo com medicamentos retirados; o benefício do medicamento sobre o “placebo” não tem significado clínico; e os cálculos do NNT revelam que oito de nove pacientes poderiam ser vistos como “prejudicados” pelo tratamento.
No entanto, o brilho dos RCTs é tal que nenhuma dessas deficiências e falhas descarrilha a descoberta binária – que os antidepressivos são mais “eficazes” do que placebo – é o que orienta o uso desses medicamentos pela sociedade. De fato, se voltarmos ao relatório Kirsch, aqui está uma ilustração do único aspecto dos dados em que a psiquiatria e a sociedade estão confiando para afirmar que as drogas são um tratamento eficaz para a depressão:

Os dados que são ignorados
Os dados do RCT são um elemento de um grande pool de dados que existe a respeito do impacto dos antidepressivos. Os vários “tipos” de dados, quando vistos separadamente, são como peças de um quebra-cabeças sobre as quais se encontra, e qualquer avaliação da base de evidência dos antidepressivos deve procurar ver como elas se encaixam entre si. Qual é o quadro geral?
Em meu livro Anatomia de uma Epidemia, e em dois ensaios anteriores para o Mad in America, juntei as peças do quebra-cabeças de uma maneira narrativa que contou como, antes da chegada dos “antidepressivos”, a depressão era entendida enquanto um transtorno episódico, e que depois que os antidepressivos se tornaram o tratamento de primeira linha a depressão começou a ter um curso crônico, com os pesquisadores apresentando uma explicação biológica para o porquê dos medicamentos poderem ter esse efeito.
O que se segue são simplesmente as peças do quebra-cabeças que existem na literatura médica (além dos RCTs), sem qualquer esforço da minha parte para tirar uma conclusão. Esta é a informação que a psiquiatria – e, portanto, a sociedade – indica quando coloca nosso foco social nos dados do RCT. O objetivo aqui é iluminar a miopia desse foco, e como ele mal serve à nossa sociedade.
O curso natural da depressão
O curso natural de uma “doença” serve como uma linha de base necessária para se avaliar se uma intervenção é útil. Por exemplo, imagine que na natureza, 50% dos pacientes atingidos por uma doença tenham se recuperado no final de um ano. Uma intervenção médica precisa produzir uma taxa de recuperação maior do que a necessária para proporcionar um benefício. Se uma intervenção médica levar a uma taxa de recuperação de um ano de 40%, os médicos – se não tiverem uma noção da taxa de recuperação natural – provavelmente verão sua intervenção como eficaz. Os 40% dos pacientes que se recuperaram também o verão dessa forma. No entanto, de fato, a intervenção médica reduziu a taxa de recuperação, um fato que permanecerá oculto sem o conhecimento do curso natural do transtorno.
Antes da introdução de antidepressivos, a depressão era entendida como um transtorno bastante incomum. Pesquisas comunitárias dos anos 30 e 40 descobriram que menos de um em mil adultos sofria de depressão clínica a cada ano. Estudos de pacientes hospitalizados contavam como os sintomas depressivos diminuíam regularmente com o tempo, e muitas vezes nunca mais voltavam.[5]
Em 1972, Samuel Guze e Eli Robins da Faculdade de Medicina da Universidade de Washington em St. Louis revisaram a literatura científica e determinaram que em estudos de acompanhamento que duraram dez anos, 50% das pessoas hospitalizadas por depressão não tiveram nenhuma recorrência de sua doença. Apenas uma pequena minoria das pessoas com depressão unipolar – uma em dez doentes crônicos – concluiu. [6]
Esta foi a evidência científica que levou os funcionários da NIMH e outros, durante as décadas de 1960 e 1970, a falar otimisticamente sobre o curso da doença a longo prazo. Aqui está uma amostra de tais pronunciamentos: [7]
- “A depressão é, de modo geral, uma das condições psiquiátricas com melhor prognóstico para uma eventual recuperação com ou sem tratamento. A maioria das depressões são autolimitadas”. -Jonathan Cole, diretor do Centro de Serviço de Psicofarmacologia do NIMH, 1964.
- “No tratamento da depressão, sempre se tem como aliado o fato de que a maioria das depressões terminam em remissões espontâneas. Isto significa que em muitos casos, independentemente do que se faça, o paciente eventualmente começará a melhorar”. -Nathan Kline, diretor de pesquisa no Rockland State Hospital em Nova York, 1964.
- A maioria dos episódios depressivos “seguirá seu curso e terminará com uma recuperação praticamente completa sem intervenção específica”. – Dean Schuyler, chefe da seção de depressão do NIMH, 1974.
De fato, a remissão espontânea era tão comum que Schuyler concluiu que seria difícil “julgar a eficácia de uma droga”. Talvez um medicamento pudesse encurtar o tempo de recuperação, já que a remissão espontânea em pacientes hospitalizados muitas vezes levava muitos meses para acontecer, mas seria quase impossível melhorar a alta taxa de remissão – 85% ou assim no final de um ano.
Resultados em pacientes do mundo real tratados com antidepressivos
Nos anos 70, as benzodiazepinas foram a droga de escolha para “ansiedade” e outros desconfortos emocionais. Os benzodiazepínicos caíram em desuso por causa de suas qualidades viciantes, e logo os antidepressivos se tornaram a droga de escolha, e isto foi particularmente verdadeiro após a chegada do Prozac em 1988.
Durante os anos 90, os psiquiatras nos Estados Unidos e em outros lugares ampliaram o espectro de resultados associados aos antidepressivos. Um terço de todos os pacientes unipolares não respondiam às drogas e tinham resultados pobres a longo prazo. Outro terço eram “respondedores parciais” aos medicamentos e, em testes de curto prazo, apareceram como sendo ajudados pelo medicamento. O problema era que estes pacientes recaíam com freqüência posteriormente. O terço final foi enviado a curto prazo, mas apenas cerca da metade ficou bem.
O livro didático de 1999 da Associação Psiquiátrica Americana resumiu este espectro de resultados:
“Apenas 15% das pessoas com depressão unipolar experimentam um único episódio da doença”, observou o livro, e para os 85% restantes, a cada novo episódio, as remissões se tornam “menos completas e novas recidivas se desenvolvem com menos provocação.” [8]
Por volta dessa época, a NIMH financiou três estudos para avaliar os resultados de um ano de pacientes “do mundo real” tratados para a depressão. Em dois dos estudos – o primeiro um estudo com 118 pacientes ambulatoriais no Texas; o segundo o grande estudo STAR*D – todos os pacientes foram tratados com antidepressivos, e ambos os protocolos foram projetados para maximizar as taxas de remissão. O terceiro foi um estudo de 84 pacientes para avaliar o “curso de depressão sem tratamento“. As taxas de remissão ao final de um ano foram as seguintes:

O investigador principal do estudo “sem tratamento”, Michael Posternak, concluiu que os resultados refletiam os resultados relatados por Emil Kraepelin quase um século antes. Kraepelin havia observado que os episódios depressivos não tratados geralmente eram esclarecidos em seis meses, e este novo estudo, escreveu ele, forneceu “talvez a confirmação metodologicamente mais rigorosa desta estimativa”.
Os pobres resultados que apareceram nos dois estudos financiados pelo NIMH foram replicados em outros cenários do “mundo real”. Por exemplo, um relatório de Minnesota sobre os resultados no mundo real de 260.000 pacientes tratados por depressão de 2011 a 2014, por provedores médicos em todo o estado, encontrou taxas de remissão igualmente baixas. No final de cada ano, apenas cerca de 5% dos pacientes estavam em remissão. Outros 10% foram considerados como respondedores ao tratamento antidepressivo (queda de 50% nos sintomas.) Os 85% restantes foram classificados como cronicamente deprimidos.

Dois estudos publicados em 2022 completam este quadro de maus resultados em pacientes do mundo real:
- Em um estudo internacional de 2022 com 1.279 pacientes, que foi financiado por Lundbeck e conduzido por investigadores com numerosos vínculos com empresas farmacêuticas, apenas 25% responderam ao tratamento antidepressivo. Os demais ou não responderam (34%) ou foram considerados “resistentes ao tratamento” depois de não responderem duas vezes a um antidepressivo (41%).
- Em um estudo com 1.944 pacientes em 22 centros médicos do Departamento de Assuntos de Veteranos (VA), que envolveu testes para possíveis interações genético-drogativas com a esperança de que pudesse aumentar as taxas de resposta, a taxa de resposta composta para os dois grupos foi de 30%, com os testes genéticos provando ser de pouco valor.
Resultados medicados vs. não medicados
Resultados medicados vs. não medicados
Durante os últimos 25 anos, pesquisadores na Europa, Canadá e Estados Unidos realizaram um pequeno número de “estudos naturalistas” que avaliaram os resultados da depressão com base no uso de antidepressivos. Essas investigações constataram regularmente que os pacientes medicados são mais propensos à depressão e ao comprometimento das funções.
Aqui estão resumos de dez desses estudos.
1) “Characteristics and Significance of Untreated Major Depressive Disorder” (1995). Investigadores financiados pela NIMH relataram que, durante um período de seis anos, aqueles que foram “tratados” pela doença tinham três vezes mais probabilidade de sofrer uma “cessação” de seu “papel social principal” e quase sete vezes mais probabilidade de ficar “incapacitados”.
Os pesquisadores da NIMH escreveram: “Os indivíduos não tratados aqui descritos tinham doenças mais leves e de duração mais curta (do que aqueles que foram tratados) e, apesar da ausência de tratamento, não mostraram mudanças significativas no status socioeconômico a longo prazo”.

2.) “Outcome of Anxiety and Depressive Disorders in Primary Care” (1997). Em um estudo britânico com 148 pacientes deprimidos, o grupo nunca-medicado viu seus sintomas diminuir em 62% em seis meses, enquanto os pacientes tratados com medicamentos experimentaram apenas uma redução de 33% nos sintomas.
3. “The Effects of Detection and Treatment on the Outcome of Major Depression in Primary Care” (1998). Um estudo da Organização Mundial da Saúde sobre pacientes deprimidos em 15 cidades do mundo descobriu que, ao final de um ano, aqueles que não estavam expostos a medicamentos psicotrópicos desfrutavam de uma saúde geral muito melhor, seus sintomas depressivos eram muito mais suaves e era menos provável que ainda estivessem “doentes mentais”.

4. “Treatment of Depression Related to Recurrence” (2000). Em um estudo retrospectivo de 10 anos de resultados, os investigadores holandeses descobriram que 76% dos que não foram tratados com um antidepressivo recuperaram e nunca recaíram, em comparação com 50% dos que foram prescritos com um antidepressivo.
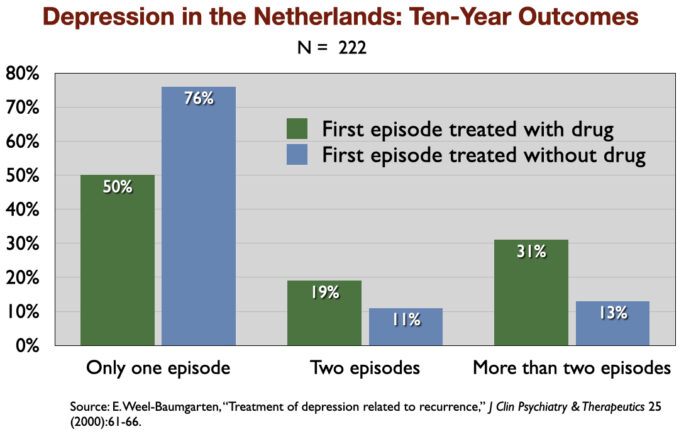
5. “Pattern of Antidepressant Use and Duration of Depression-Related Absence from Work” (2003). Os investigadores canadenses identificaram 1.281 pessoas que ficaram com uma incapacidade de curto prazo entre 1996 e 1998 porque perderam dez dias consecutivos de trabalho devido à depressão. Aqueles que não receberam a prescrição de um antidepressivo voltaram ao trabalho, em média, em 77 dias, enquanto o grupo medicado levou 105 dias para voltar ao trabalho. Apenas 9% do grupo não medicado passou para incapacidade prolongada, em comparação com 19% daqueles que tomaram um antidepressivo.

6. “The Impact of Antidepressant Treatment on Population Health” (2004). Em um estudo de cinco anos com 9.508 pacientes deprimidos no Canadá, os pacientes medicados estavam deprimidos em média 19 semanas por ano, contra 11 semanas para aqueles que não tomavam os medicamentos. Os investigadores canadenses concluíram que “o tratamento antidepressivo pode levar a uma deterioração no curso a longo prazo dos transtornos de humor”.
7. “Continuation and Maintenance Use of Antidepressants in Recurrent Depression” (2008). Pesquisadores na Holanda acompanharam 172 pacientes durante dois anos após sua depressão ter entrado em remissão, e descobriram que durante esse acompanhamento a taxa de recidivas foi de 60% para aqueles que tomaram continuamente um antidepressivo, 64% para aqueles que tomaram intermitentemente um, e 26% para aqueles que não tomaram nenhum antidepressivo.

8. “Impact of Duration of Antidepressant Treatment on the Risk of a New Sequence of Antidepressant Treatment” (2011). Pesquisadores franceses, em um estudo com 35.000 pacientes do primeiro episódio, descobriram que quanto mais tempo os pacientes eram tratados com um antidepressivo antes de se retirarem do medicamento, maior a taxa de recidiva. Aqueles que foram expostos a um antidepressivo por mais de seis meses tinham mais que o dobro do risco de recaída do que aqueles expostos por menos de um mês.
9. “Poorer Long-Term Outcomes Among Persons with Major Depressive Disorder Treated with Medication” (2017). Uma análise dos resultados de 3.294 pessoas que foram diagnosticadas com depressão e seguiram por nove anos revelou que aqueles que tomaram antidepressivos durante esse período tiveram sintomas mais graves ao final de nove anos do que aqueles que não tomaram tal medicação. A diferença nos resultados não poderia ser explicada por nenhuma diferença na gravidade inicial da depressão.
10) “Antidepressant Use Prospectively Relates to a Poorer Long-Term Outcome of Depression” (2018). Um estudo prospectivo de 521 pacientes deprimidos na Suíça, que foram acompanhados dos 20 aos 50 anos de idade, descobriu que tomar um antidepressivo em algum momento durante esse período estava associado a resultados piores no final do estudo, mesmo quando se controlava os sintomas iniciais e outros fatores.
Efeitos adversos
O NNT que emerge dos RCTs de antidepressivos informa como oito dos nove pacientes deprimidos tratados com um antidepressivo não recebem nenhum benefício do medicamento (em termos de redução de sintomas além do placebo), e ainda estão expostos aos perigos do medicamento.
A lista de efeitos colaterais conhecidos associados aos antidepressivos é longa. Ela inclui numerosos efeitos adversos físicos, emocionais e psiquiátricos. O maior risco, entretanto, é que a exposição a um antidepressivo leve a um agravamento a longo prazo: uma conversão para transtorno bipolar, disfunção sexual persistente, e depressão crônica. Dificuldades na retirada de antidepressivos aumentam a probabilidade de que uma prescrição inicial venha a evoluir para o uso a longo prazo.
Há muito se sabe que os antidepressivos podem desencadear um episódio maníaco. Este é um “efeito adverso” que pode converter a depressão “unipolar” em um diagnóstico bipolar. Em um trabalho de 2002, pesquisadores da Universidade de Yale quantificaram o risco durante um período de dez meses: um de cada 12 pacientes deprimidos expostos a antidepressivos se converterá em bipolar, que é o dobro da taxa de conversão em pacientes deprimidos não expostos aos medicamentos.

Até 75% dos usuários de ISRS relatam algum grau de disfunção sexual – baixa libido, secura vaginal, disfunção erétil, e orgasmos menos intensos. Como os pesquisadores irlandeses escreveram, “os efeitos sexuais adversos parecem ser a regra, e não a exceção com os ISRSs”. Além disso, mesmo após a retirada de um antidepressivo ISRS, a disfunção sexual pode persistir indefinidamente, uma condição conhecida como PSSD: disfunção sexual pós-ISRS.
O risco de desenvolvimento do PSSD não é conhecido. A disfunção sexual pode, naturalmente, ser devastadora para o indivíduo. De uma perspectiva da evolução, o PSSD pode ser visto como uma pessoa que está “menos em forma” pela droga. Uma nação de pessoas em ISRSs não seria uma população próspera.
Como observado acima, na era pré-antidepressiva, a recuperação de um episódio depressivo era esperada. Após a introdução dos antidepressivos, o curso de longo prazo da depressão – como o revelado pelos estudos clínicos – começou a ter um curso mais crônico. No início dos anos 90, os pesquisadores relataram que 10% a 15% dos pacientes diagnosticados com depressão grave tinham se tornado “resistentes ao tratamento”. Este mau resultado continuou a aumentar à medida que os ISRSs foram popularizados, de tal forma que uma pesquisa de 2006 concluiu que quase 40% dos pacientes deprimidos que tomaram antidepressivos por um período mais longo acabaram “resistentes ao tratamento”.
Com a depressão correndo um curso mais crônico, e quase 40% dos pacientes acabando “resistentes ao tratamento”, o psiquiatra italiano Giovanni Fava e um punhado de outros propuseram uma explicação biológica para este declínio nos resultados: O ISRS e outros antidepressivos induzem mudanças no cérebro que tornam os pacientes mais vulneráveis biologicamente à depressão.
Em um artigo de 2011, El-Mallakh, especialista em transtornos do humor na Faculdade de Medicina da Universidade de Louisville, resumiu a hipótese:
“Um estado depressivo crônico e resistente ao tratamento é proposto para ocorrer em indivíduos que são expostos a antagonistas potentes de bombas de recaptação de serotina (ISRSs) por períodos de tempo prolongados. Devido ao atraso no aparecimento deste estado depressivo crônico, ele é rotulado como disforia tardia. A disforia tardia manifesta-se como um estado disfórico crônico que é inicialmente aliviado de forma transitória – mas que acaba por se tornar uma medicação antidepressiva que não responde. Os antidepressivos serotonérgicos podem ser de particular importância no desenvolvimento da disforia tardia”.
Ele concluiu que a disforia tardia induzida pela droga poderia “continuar por um período de tempo após a interrupção do medicamento, e pode não ser reversível”.
Enquanto muitas pessoas expostas a antidepressivos são capazes de deixar as drogas sem muita dificuldade após um período mais curto de uso, o uso prolongado pode levar a uma “síndrome de descontinuação” quando as pessoas tentam sair do medicamento. Os sintomas de abstinência, os pesquisadores escreveram em um artigo de 2022, incluem sintomas semelhantes aos da gripe, ansiedade, capacidade emocional, diminuição do humor, irritabilidade, crises de choro, tonturas, tremores, fadiga e sensações de choque elétrico. Os sintomas geralmente persistem por semanas e podem durar meses ou mesmo anos. Metade dos pacientes que sofrem efeitos de abstinência classificam os sintomas como “graves”.
Resultados da Saúde Pública
Se os antidepressivos “funcionassem”, o público poderia esperar que o aumento da prescrição desses medicamentos nos últimos 30 anos teria reduzido a “carga social da depressão”. Eles teriam proporcionado um benefício de saúde pública: a carga econômica diminuiria (pois mais pessoas poderiam trabalhar); a taxa de suicídio diminuiria; e as taxas de incapacidade diminuiriam.
No entanto, o oposto provou ser verdade.
Uso de antidepressivos
O uso de antidepressivos tem aumentado constantemente desde que o Prozac foi introduzido em 1988. A porcentagem de adultos americanos com 12 anos ou mais que usaram um antidepressivo no “mês anterior” saltou sete vezes durante este período de 30 anos.
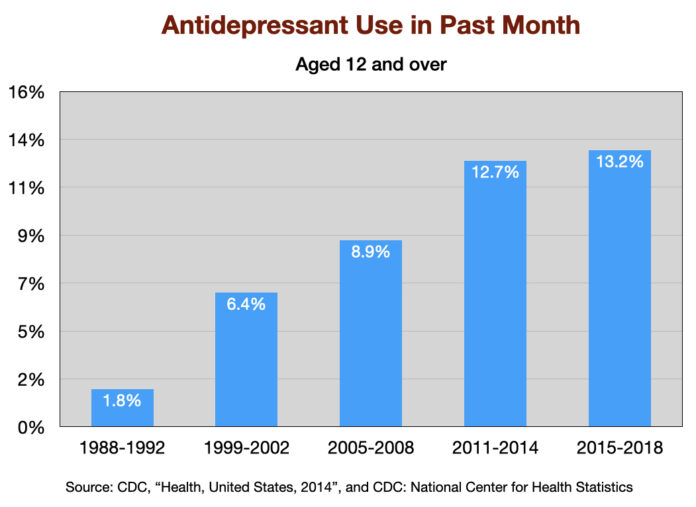
Carga econômica da depressão
Em 1990, a “carga econômica” da depressão nos EUA foi calculada em 116 bilhões de dólares (em dólares de 2020). Esta cifra é composta de gastos diretos em terapia e medicamentos, bem como cuidados residenciais nas instalações; custos relacionados ao suicídio; e custos no local de trabalho (perda de produtividade devido à depressão.) Esta carga econômica aumentou três vezes desde então, atingindo 326 bilhões de dólares em 2018 (em dólares de 2020).

Taxas de suicídio
Há uma série de fatores associados à mudança das taxas de suicídio, com a posse de armas e o desemprego, dois fatores principais. A taxa de suicídio diminuiu nos anos 90, e depois aumentou de forma constante durante as duas décadas seguintes.

Espera-se que os antidepressivos sirvam como um fator que reduza a taxa de suicídio. Entretanto, dois grandes estudos de coorte de pacientes deprimidos em ambientes de cuidados primários (um nos EUA e outro no Reino Unido) relataram taxas de suicídio muito mais altas para pacientes deprimidos que tomaram um antidepressivo. Um terceiro estudo no Reino Unido de pacientes deprimidos do primeiro episódio encontrou uma taxa de suicídio muito mais alta enquanto tomavam o medicamento ou durante as primeiras quatro semanas após o abandono do medicamento (período de abstinência do medicamento).
Da mesma forma, um grande estudo com veteranos americanos diagnosticados com um problema de saúde mental encontrou uma taxa de suicídio 50% mais alta naqueles que foram tratados para o problema.

O boom bipolar
O rápido aumento na prescrição de ISRSs nos anos 90 foi acompanhado por um notável aumento na prevalência de doenças bipolares em nossa sociedade. No curto período de uma década (1992-2003), a prevalência da bipolaridade em adultos quase dobrou, e aumentou 40 vezes na juventude.
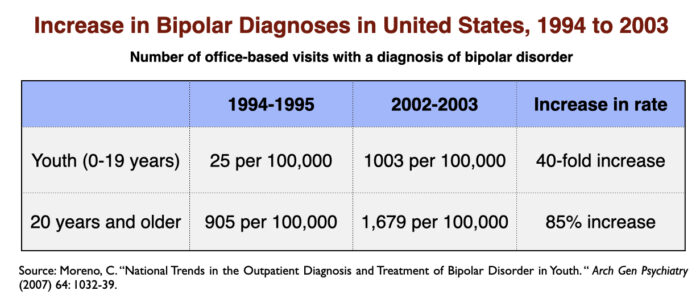
Embora a expansão dos limites diagnósticos tenha contribuído para este espantoso aumento da doença bipolar, uma pesquisa com membros da Depressive and Manic-Depressive Association constatou que 60% dos que tinham um diagnóstico bipolar tinham inicialmente apresentado uma grande depressão e tinham se tornado bipolares após a exposição a um antidepressivo.
Em nível de saúde pública, o aumento do número de pacientes “bipolares” revela um agravamento da saúde mental da sociedade. Bipolar é entendido como um transtorno mais grave do que a depressão ou qualquer outro transtorno de humor; diz-se que 85% sofrem de “deficiência grave”.
Ascensão das taxas de Incapacidade
Dois dos estudos citados acima na seção sobre “resultados medicados versus não medicados” encontraram taxas mais altas de incapacidade para pacientes deprimidos que tomaram antidepressivos em comparação com aqueles que não tomaram. A nível social, esses estudos serviram como uma previsão de que a incapacidade devido a transtornos do humor aumentaria com o aumento do uso de antidepressivos. Esse aumento apareceu rapidamente nos anos 90, quando os ISRSs se tornaram os medicamentos mais vendidos.
Enquanto a porcentagem de adultos americanos que sofriam de transtornos de humor não mudou de 1991 para 2002, a porcentagem que recebeu tratamento, mudou. Em outras palavras, a prevalência de transtornos de humor permaneceu a mesma; a diferença foi que o número de adultos tratados por um transtorno de humor aumentou de 11,2 milhões em 1991 para 21,4 milhões em 2002. Como isto ocorreu, o número de adultos que receberam um pagamento federal por incapacidade – SSI ou SSDI – devido a um transtorno de humor saltou de 292.000 para 940.000. No curto espaço de uma década, a taxa de incapacidade para adultos com transtornos de humor subiu de 1 em 188 para 1 em 69.

Em 2016, um grupo de trabalho no Parlamento do Reino Unido me convidou para fazer uma apresentação sobre o aumento da incapacidade devido a transtornos de humor, já que isso estava ocorrendo também no Reino Unido. Naquela época, eu coletava dados sobre aumentos no uso de antidepressivos e taxas de incapacidade em seis países.





 Tais são os resultados de saúde pública associados ao aumento do uso de antidepressivos nos últimos 30 anos. A carga econômica da depressão mais do que dobrou; a taxa de suicídio aumentou constantemente durante as duas últimas décadas; houve um “boom bipolar”, e as taxas de incapacidade devido a distúrbios de humor dispararam em país após país que adotou o uso generalizado das drogas.
Tais são os resultados de saúde pública associados ao aumento do uso de antidepressivos nos últimos 30 anos. A carga econômica da depressão mais do que dobrou; a taxa de suicídio aumentou constantemente durante as duas últimas décadas; houve um “boom bipolar”, e as taxas de incapacidade devido a distúrbios de humor dispararam em país após país que adotou o uso generalizado das drogas.
Os Pedaços de um Quebra-cabeça
Como escrevi anteriormente, os vários tipos de provas relativas ao impacto dos antidepressivos são como as peças de um quebra-cabeça. A esperança é que as peças se encaixem para apresentar uma imagem clara “baseada em evidências” de seus méritos.
Neste caso, aqui estão as peças do quebra-cabeça:
- Nos RCTs, os antidepressivos proporcionam uma redução “estatisticamente significativa” maior dos sintomas a curto prazo, em comparação com o placebo.
- A diferença na redução dos sintomas é tão pequena que é clinicamente insignificante e não seria perceptível por clínicos ou pacientes.
- A maioria dos RCTs são financiados pela indústria e tendenciosos de maneiras que favorecem o medicamento.
- Com base nos cálculos do “tamanho do efeito”, oito de nove pacientes não se beneficiarão do tratamento antidepressivo (além do placebo), e ainda assim serão expostos a efeitos adversos associados ao seu uso.
- Na era pré-antidepressiva, a depressão era entendida como um curso episódico. A maioria das pessoas poderia esperar uma recuperação. Uma vez que os antidepressivos foram popularizados, a depressão começou a ter um curso mais crônico.
- Estudos no “mundo real” de pacientes descobrem que apenas 25% a 30% “respondem” a um antidepressivo, e que as taxas de remissão ao final de um ano são muito mais baixas (abaixo de 15%).
- Um estudo destinado a avaliar as taxas de recuperação em pacientes “sem tratamento” relatou que 85% estavam bem no final do ano, semelhante aos resultados da era pré-antidepressiva.
- Estudos naturalistas que avaliam os resultados de acordo com o uso de antidepressivos descobrem regularmente que o grupo medicado tem resultados piores: é mais provável que permaneçam sintomáticos e mais provável que fiquem incapacitados pelo distúrbio.
- No nível da saúde pública, o peso dos transtornos depressivos tem aumentado acentuadamente durante os últimos 30 anos.
A conclusão de que o trabalho com “antidepressivos” vem da peça número um do quebra-cabeça . . . Os RCTs provaram que os antidepressivos produzem um benefício “estatisticamente significativo” em relação ao placebo a curto prazo, e o resto da informação pode ser descartada. A desconstrução dos RCTs é colocada no fundo da conversa, e o restante das informações é descartado como inferior aos estudos dos RCTs.
Tal é a miopia que orienta o uso de antidepressivos pela sociedade.
Um quadro muito diferente, é claro, emerge quando as peças do quebra-cabeças dois a nove são incorporadas à “base de provas”. Essas peças se juntam para contar os danos causados e, pode-se argumentar, os danos em uma vasta escala. Mesmo os dados da RCT agora acrescentam a essa conclusão: eles falam de drogas que, em testes tendenciosos por projeto para favorecer a droga, não conseguem fornecer um benefício clinicamente significativo a curto prazo. Se você tirar os antolhos, a literatura científica conta uma história muito robusta sobre a eficácia dos antidepressivos e o seu impacto sobre a saúde pública.
Notas de Rodapé
- J. Cornwall, The Power to Harm (New York: Viking, 1996):147-48.
- D. Graham, “Sponsor’s ADR submission on fluoxetine dated July 17, 1990,” FDA document, September 1990.
- P. Breggin, Talking Back to Prozac (New York: St Martin’s Press, 1994): 90
- R. Whitaker and L. Cosgrove, Psychiatry Under the Influence (New York: Palgrave Macmillan, 2015):75
- R. Whitaker, Anatomy of an Epidemic (New York: Broadway Books, 2010):150-153.
- D. Schuyler, The Depressive Spectrum (New York: Jason Aronsom, 1974) 49.
- Whitaker, ibid, 153.
- R. Hales, editor, Textbook of Psychiatry (Washington D.C.: American Psychiatric Press, 1999):547.
[trad. e edição Fernando Freitas]










